
【题目】到目前为止,由化学能转变的热能或电能仍然是人类使用最广泛的能源.
(1)在25℃、101kPa下,16g的甲烷完全燃烧生成CO2和液态水时放出a kJ(a>0)的热量,则表示甲烷燃烧热的热化学方程式为 .
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关. ①图1是N2(g)和H2(g)发生反应生成1mol NH3(g)过程中的能量变化示意图,该反应过程是(填“放热”或“吸热”)过程,请写出生成2mol NH3的热化学方程式: . 
②已知:
化学键 | H﹣H | N≡N |
键能(kJ/mol) | 435 | 943 |
试根据上表及图1中的数据计算N﹣H键的键能为kJ/mol.
③若起始时向容器内放入1mol N2和3mol H2 , 10分钟后N2的转化率为15%,则该反应进行到此时共放出的热量为kJ.
(3)①二氧化碳的捕集、利用是我国能源领域的一个重要研究方向.工业上用CO2和H2反应合成二甲醚.已知: CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H1=﹣53.7kJ/mol
CH3OCH3(g)+H2O (g)═2CH3OH(g)△H2=+23.4kJ/mol
则:2CO2(g)+6H2(g)CH3OCH3 (g)+3H2O(g)△H3=kJ/mol.
【答案】
(1)CH4(g)+3O2(g)═CO2(g)+2H2O (l)△H=﹣2aKJ/mol
(2)放热;N2(g)+3H2(g)=2NH3(g)△H=﹣92KJ/mol;390;13.8
(3)﹣130.8
【解析】解:(1)16g的甲烷(CH4)即1mol完全燃烧生成CO2和液态水时放出akJ的热量,标注物质聚集状态和对应焓变写出热化学方程式为:CH4(g)+3O2(g)═CO2(g)+2H2O (l)△H=﹣2aKJ/mol;所以答案是:CH4(g)+3O2(g)═CO2(g)+2H2O (l)△H=﹣2aKJ/mol;(2)①有图可知,反应物总能量大于生成物总能量,则该反应为放热反应;又焓变等于反应物活化能减去生成物活化能求算焓变,所以N2(g)和H2(g)发生反应生成1mol NH3(g)过程中的△H=254KJ/mol﹣300KJ/mol=﹣46KJ/mol,所以生成2mol NH3的热化学方程式为N2(g)+3H2(g)=2NH3(g)△H=﹣46KJ/mol×2=﹣92KJ/mol,所以答案是:放热;N2(g)+3H2(g)=2NH3(g)△H=﹣92KJ/mol;②反应热等于反应物的总键能减去生成物的总键能,设N﹣H的键能为x,则943+3×435﹣6x=﹣92,x=390,所以答案是:390;③因为放入1mol N2和3mol H2 , 10分钟后N2的转化率为15%,所以消耗氮气为0.15mol,又N2(g)+3H2(g)=2NH3(g)△H=﹣92KJ/mol,则放出的热量为0.15mol×92KJ/mol=13.8KJ,所以答案是:13.8;(3)已知:Ⅰ.CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H1=﹣53.7kJmol﹣1Ⅱ.CH3OCH3(g)+H2O(g)═2CH3OH(g)△H2=+23.4kJmol﹣1根据盖斯定律,Ⅰ×2﹣Ⅱ可得:2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g),△H3=2△H1﹣△H2=2×(﹣53.7kJmol﹣1)﹣23.4kJmol﹣1=﹣130.8kJmol﹣1 , 所以答案是:﹣130.8.
【考点精析】关于本题考查的反应热和焓变,需要了解在化学反应中放出或吸收的热量,通常叫反应热才能得出正确答案.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】利用下列实验装置进行的相应实验,不能达到实验目的是( ) 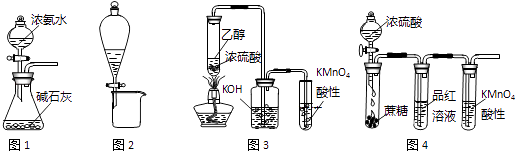
A.图1装置可制取氨气
B.图2装置可分离CH3COONa和CH3COOC2H5混合液
C.图3所示装置可制取乙烯并验证其易被氧化
D.图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)俗称保险粉,可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。实验室可通过如下反应制取:2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2。
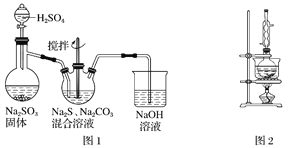
(1)用图1所示装置制取Na2S2O3,其中NaOH溶液的作用是________________________。如将分液漏斗中的H2SO4改成浓盐酸,则三颈烧瓶内除生成Na2S2O3外,还有________(填化学式)杂质生成。
(2)为测定所得保险粉样品中Na2S2O3·5H2O的质量分数,可用标准碘溶液进行滴定,反应方程式为2Na2S2O3+I2===2NaI+Na2S4O6。
①利用KIO3、KI和HCl可配制标准碘溶液。写出配制时所发生反应的离子方程式:_______________________________________________________________________。
②准确称取一定质量的Na2S2O3·5H2O样品于锥形瓶中,加水溶解,并滴加________作指示剂,用所配制的标准碘溶液滴定。滴定时所用的玻璃仪器除锥形瓶外,还有________。
③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的质量分数的测量结果________(填“偏高”、“偏低”或“不变”)。
(3)本实验对Na2S的纯度要求较高,利用图2所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯步骤如下,请填写实验操作。
①将已称量好的工业Na2S放入圆底烧瓶中,并加入一定质量的酒精和少量水;
②按图2所示组装所需仪器,向冷凝管中通入冷却水,水浴加热;
③待________________时,停止加热,将烧瓶取下;
④____________________________________________________________________;
⑤____________________________________________________________________;
⑥将所得固体洗涤、干燥,得到Na2S·9H2O晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2 . 在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g.下列有关说法不正确的是( )
A.Cu与Cu2O的物质的量之比为2:1
B.硝酸的物质的量浓度为2.6mol/L
C.产生的NO在标准状况下的体积为4.48L
D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、U、W五种短周期非金属元素,它们的原子半径与原子序数有如图关系,化合物XZ是水煤气的主要成分之一,下列说法不正确的是
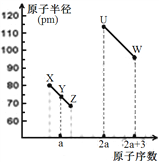
A. U、X、W 三种元素最高价氧化物对应的水化物酸性依次增强
B. 由Y、Z和氢三种元素形成的化合物中一定只含共价键
C. XZ2与X60的化学键类型和晶体类型都相同
D. X的位置是第2周期、第ⅣA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应中的能量变化,表述正确的是( )
A.放热反应中,反应物的总能量大于生成物的总能量
B.断开化学键的过程会放出能量
C.加热才能发生的反应一定是吸热反应
D.酸碱中和反应都是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42﹣等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列有关对该溶液的判断不正确的是( )

A. 该溶液中肯定含有的离子是H+、NH4+、Al3+、SO42﹣
B. 肯定不含的阳离子是Mg2+、Fe3+
C. 要确定该溶液是否含有Na+,必须做焰色反应实验,看焰色是否为黄色
D. 该溶液中肯定含有的离子的物质的量之比为n(H+):n(NH4+):n(Al3+):n(SO42﹣)=2:3:1:4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com