
工业上可用食盐和石灰石为主要原料,经不同的方法生产纯碱。请回答下列问题:
(1)卢布兰芳是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取,结晶而制得纯碱。
①食盐和浓硫酸反应的化学方程式为 ;
②硫酸钠和焦炭、石灰石反应的化学方程式为_ (已知产物之一为CaS);
(2)氨碱法的工艺如下图所示,得到的碳酸氢钠经煅烧生成纯碱。
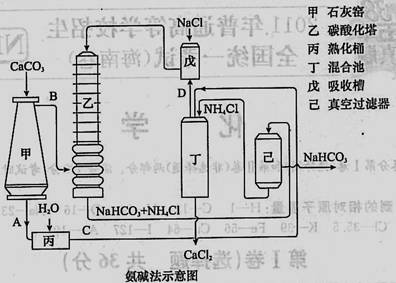
①图中的中间产物C是_______,D_______。(写化学式);
②装置乙中发生反应的化学方程式为 ;
(3)联合制碱法对氨碱法的改进,其优点是 ;
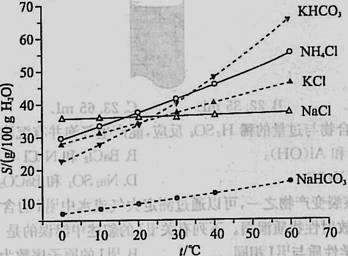
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石为原料制碳酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行? 。
【知识点】纯工业(侯氏制碱)
【答案解析】 (1)①NaCl+H2SO4(浓)=NaHSO4+HCl↑
或2NaCl+H2SO4(浓)  Na2SO4+2HCl↑(2分)
Na2SO4+2HCl↑(2分)
②Na2SO4+ 2C+CaCO3 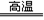 CaS+Na2CO3+2CO2↑ (2分)
CaS+Na2CO3+2CO2↑ (2分)
(2)Ca(OH)2(2分) NH3(2分)②NH3 + CO2 +NaCl +H2O = NaHCO3↓+ NH4Cl (2分)
(3)提高食盐利用率、副产物氯化铵可用作化肥、可利用合成氨的产物CO2。 (2分)
(4)不可行(1分) 因为KHCO3的溶解度较大,且在常温下与KCl溶解度相差小,在铵盐水碳酸化时无法大量析出。(2分)
解析:(1)①根据难挥发性酸制备挥发性酸的原理,浓硫酸与氯化钠晶体反应生成HCl气体,反应方程式为: NaCl+H2SO4(浓)=NaHSO4+HCl↑或2NaCl+H2SO4(浓)  Na2SO4+2HCl↑(2分);②硫酸钠和焦炭、石灰石反应的产物之一为CaS,说明发生了氧化还原反应,S元素的化合价降低,Na2SO4作氧化剂,则作还原剂的为焦炭,C元素的化合价升高为+4价,由此可判断产物还有碳酸钠和二氧化碳,其反应方程式为Na2SO4+ 2C+CaCO3
Na2SO4+2HCl↑(2分);②硫酸钠和焦炭、石灰石反应的产物之一为CaS,说明发生了氧化还原反应,S元素的化合价降低,Na2SO4作氧化剂,则作还原剂的为焦炭,C元素的化合价升高为+4价,由此可判断产物还有碳酸钠和二氧化碳,其反应方程式为Na2SO4+ 2C+CaCO3 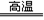 CaS+Na2CO3+2CO2↑ ;(2)①甲装置为煅烧石灰石生成氧化钙和二氧化碳的装置,生成的氧化钙与水反应生成氢氧化钙,所以C应为Ca(OH)2,Ca(OH)2加入到丁装置,与NH4Cl反应生成NH3,则D应为NH3; ②在溶液中足量的CO2和H2O及NH3会生成HCO3-,HCO3-再与Na+结合生成NaHCO3晶体,以沉淀的形式析出,故答案为:NaCl+CO2+H2O+NH3=NaHCO3↓+NH4Cl
CaS+Na2CO3+2CO2↑ ;(2)①甲装置为煅烧石灰石生成氧化钙和二氧化碳的装置,生成的氧化钙与水反应生成氢氧化钙,所以C应为Ca(OH)2,Ca(OH)2加入到丁装置,与NH4Cl反应生成NH3,则D应为NH3; ②在溶液中足量的CO2和H2O及NH3会生成HCO3-,HCO3-再与Na+结合生成NaHCO3晶体,以沉淀的形式析出,故答案为:NaCl+CO2+H2O+NH3=NaHCO3↓+NH4Cl
(3)该方法能提高原料的利用率,减少废渣的排放,保留了氨碱法的优点,消除了它的缺点,使食盐的利用率提高;NH4Cl 可做氮肥;可与合成氨厂联合,使合成氨的原料气 CO 转化成 CO2,革除了 CaCO3 制 CO2 这一工序.
故答案为:提高食盐利用率、副产物氯化铵可用作化肥、可利用合成氨的产物CO2。
(4)由溶解曲线图可知KHCO3和NH4Cl的溶解度相差不大,当温度高于40℃时,由图象可知,降温结晶时会析出较多的KCl;
【思路点拨】本题以工艺流程为依托,综合考查了氧化还原反应、物质的溶解性、化学实验等知识,综合性较强,有一定难度。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
某溶液中含有HCO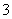 、CO
、CO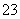 、SO
、SO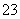 、Na+、NO
、Na+、NO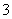 五种离子。若向其中加入Na2O2粉末充分反应后(溶液体积变化忽略不计),
五种离子。若向其中加入Na2O2粉末充分反应后(溶液体积变化忽略不计), 溶液中离子浓度保持不变的是
溶液中离子浓度保持不变的是
A.NO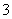 B.CO
B.CO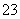 、NO
、NO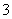
C.SO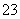 、NO
、NO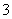 D.CO
D.CO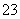 、NO
、NO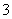 、Na+
、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g) 2c(g);ΔH1<0
2c(g);ΔH1<0
x(g)+3y(g) 2z(g);ΔH2>0
2z(g);ΔH2>0
进行相关操作且达到平衡后(忽略体积改变所作的功),下列叙述错误的是( )
A.等压时,通入惰性气体,c的物质的量不变
B.等压时,通入z气体,反应器中温度升高
C.等容时,通入惰性气体,各反应速率不变
D.等容时,通入z气体,y的物质的量浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,1 mol X和n mol Y在体积为2 L的密闭容器中发生如下反应:X(g)+Y(g)  2Z(g)+M(s),5 min后达到平衡,此时生成2a mol Z。下列说法正确的是 ( )。
2Z(g)+M(s),5 min后达到平衡,此时生成2a mol Z。下列说法正确的是 ( )。
A.用X表示此反应的反应速率是(0.1-2a) mol·L-1·min-1
B.当混合气体的质量不再发生变化时,说明反应达到平衡状态
C.向平衡后的体系中加入1 mol M,平衡向逆反应方向移动
D.向上述平衡体系中再充入1 mol X,v正增大,v逆减小,平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
向甲乙两个容积均为1 L的恒容容器中,分别充入2 mol A、2 mol B和1 mol A、1 mol B。相同条件下(温度T ℃),发生下列反应:A(g)+B(g)xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示:
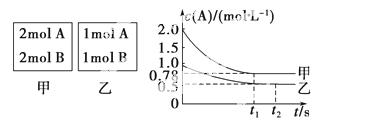
回答下列问题:
(1)乙容器中,平衡后物质B的转化率为________。
(2)x=________。
(3)T ℃时该反应的平衡常数为________。
(4)下列说法正确的是( )。
A.向平衡后的乙容器中充入氦气可使c(A)增大
B.将乙容器单独升温可使乙容器内各物质的体积分数与甲容器内相同
C.若向甲容器中再充入2 mol A、2 mol B,则平衡时甲容器中0.78 mol·L-1<c(A)<1.56 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在2 L恒容密闭容器中发生反应:2N2O5(g)  4NO2(g)+O2(g) ΔH>0。反应物和部分生成物的物质的量随反应时间变化的曲线如图73所示,下列说法正确的是( )
4NO2(g)+O2(g) ΔH>0。反应物和部分生成物的物质的量随反应时间变化的曲线如图73所示,下列说法正确的是( )
A.10 min时,反应达到平衡
B.达到平衡时N2O5的转化率为60%
C.0~20 min内平均反应速率v(N2O5)=0.05 mol·L-1·min-1
D.曲线a表示NO2的物质的量随反应时间的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
用CaSO4代替O2与燃料CO反应,既可以提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
①1/4CaSO4(s)+CO(g) 1/4CaS(s)+CO2(g) △H1=-47.3kJ/mol
1/4CaS(s)+CO2(g) △H1=-47.3kJ/mol
②CaSO4(s)+CO(g) CaO(s)+ CO2(g)+ SO2(g) △H2=+210.5kJ/mol
CaO(s)+ CO2(g)+ SO2(g) △H2=+210.5kJ/mol
③CO(g) 1/2C(s)+1/2CO2(g) △H3=-86
1/2C(s)+1/2CO2(g) △H3=-86 .2kJ/mol
.2kJ/mol
(1)反应2 CaSO4(s)+7CO(g) CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H= (用△H1△H2△H3表示)。
CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)的△H= (用△H1△H2△H3表示)。
(2)反应①~③的平衡常数的对数lgK随反应温度T的变化曲线见图18.结合各反应的△H,归纳lgK~T曲线变化规律:
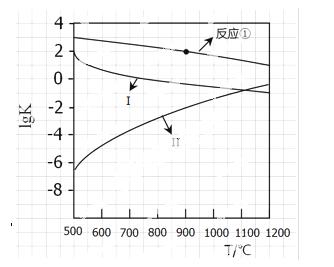
a)
b)
(3)向盛有CaSO4的真空恒容容器中充入CO,反应①于900 ºC达到平衡,c平衡(CO)=8.0×10-5mol·L-1,计算CO的转化率(忽略副反应,结果保留2位有效数字)。
(4)为减少副产物,获得更纯净的CO2,可在初始燃料中适量加入 。
(5)以反应①中生成的CaS为原料,在一定条件下经原子利用率100%的高温反应,可再生成CaSO4,该反应的化学方程式为 ;在一定条件下CO2可与对二甲苯反应,在其苯环上引入一个羧基,产物的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
T ℃时,在1 L的密闭容器中充入2 mol CO2和6 mol H2,一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得H2和CH3OH(g)的浓度随时间变化如下表所示。下列说法不正确的是( )
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,测得H2和CH3OH(g)的浓度随时间变化如下表所示。下列说法不正确的是( )
| 时间/min | c(H2)/mol·L-1 | c(CH3OH)/mol·L-1 | v(正)和v(逆)比较 |
| t0 | 6 | 0 | ? |
| t1 | 3 | 1 | v(正)=v(逆) |
A.t0~t1时间内v(H2)=3/(t1-t0) mol·L-1·min-1
B.t1时,若升高温度或再充入CO2气体,都可以提高H2的转化率
C.t0时,v(正)>v(逆)
D.T ℃时,平衡常数K=1/27,CO2与H2的转化率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质分类的说法正确的是( )
A.金刚石、白磷都属于单质
B.漂白粉、石英都属于纯净物
C.氯化铵、次氯酸都属于强电解质
D.葡萄糖、蛋白质都属于高分子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com