
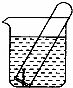
如图所示,水槽中试管内有一枚铁钉,放置数天观察:
(1)铁钉在逐渐生绣.
(2)若试管内液面上升,发生 腐蚀,电极反应:负极: ,正极:
(3)若试管内液面下降,则原溶液呈酸性,发生的电极反应:负极: ,正极: .
考点: 金属的电化学腐蚀与防护.
专题: 电化学专题.
分析: 生铁中含有碳,铁、碳和合适的电解质溶液构成原电池,在弱酸性或中性条件下,铁发生吸氧腐蚀,负极上铁失电子发生氧化反应,正极上氧气得电子和水反应生成氢氧根离子,在酸性条件下,铁发生析氢腐蚀,负极上铁失电子发生氧化反应,正极上氢离子得电子发生还原反应.
解答: 解:生铁中含有碳,铁、碳和合适的电解质溶液构成原电池,
(2)若试管内液面上升,说明试管内气体因和水反应而使其压强减小,发生的是吸氧腐蚀,铁作负极,负极上铁失电子发生氧化反应,电极反应式为:Fe﹣2e﹣=Fe2+,正极上氧气得电子发生还原反应,电极反应式为2H2O+O2+4e﹣=4OH﹣,
故答案为:吸氧,Fe﹣2e﹣=Fe2+,2H2O+O2+4e﹣=4OH﹣;
(3)若试管内液面下降,说明金属的腐蚀中生成气体导致压强增大,则金属发生的是析氢腐蚀,溶液呈酸性,负极上铁失电子发生氧化反应,电极反应式为:Fe﹣2e﹣=Fe2+,正极上氢离子得电子发生还原反应,电极反应式为:
4H++4e﹣=2H2↑,
故答案为:酸,Fe﹣2e﹣=Fe2+,4H++4e﹣=2H2↑.
点评: 本题考查了钢铁的电化学腐蚀,注意酸性条件下,钢铁发生析氢腐蚀,弱酸性或中性条件下,钢铁发生吸氧腐蚀.


科目:高中化学 来源: 题型:
①同温、同压下,质量相等的SO2和CO2相比较,体积之比为 ,
已知SO2和CO2均为酸性氧化物,写出CO2与足量NaOH溶液反应的离子方程式 ;
②某溶液中可能含有大量下列阴离子:OH﹣、SO42﹣、CO32﹣、Cl﹣.
(1)当溶液中存在大量H+时,则溶液中不可能有 .
(2)当溶液中有大量的Ba2+存在时,则溶液中不可能有 ,用离子方程式写出不可能存在的原因 、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
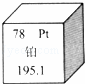
铂用于制造首饰、特种容器和标准量具衡具.如图是元素周期表提供的铂元素的部分信息,下列有关铂的说法中不正确的是( )
|
| A. | 原子序数是78 | B. | 属于非金属元素 |
|
| C. | 元素符号是Pt | D. | 相对原子质量是195.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于如图所示装置的叙述,正确的是()
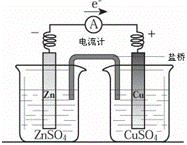
A. 铜是阳极,铜片上有气泡产生
B. 铜片质量逐渐减少
C. 电流从锌片经导线流向铜片
D. 铜离子在铜片表面被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
若某装置(电解池或原电池)中发生的总反应的离子方程式是Cu+2H+═Cu2++H2↑,则下列关于该装置的有关说法中正确的是()
A. 该装置可能是原电池,也可能是电解池
B. 该装置只能是原电池,且电解质溶液为硝酸
C. 该装置只能是电解池,且金属铜为该电解池的阳极
D. 该装置只能是原电池,电解质溶液不可能是盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
可以用来鉴别己烯、甲苯、乙酸乙酯、苯酚溶液的一组试剂是()
A. 氯化铁溶液 溴水
B. 碳酸钠溶液 溴水
C. 酸性高锰酸钾溶液 溴水
D. 酸性高锰酸钾溶液 氯化铁溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是()

A. 分子式为C7H6O5
B. 1mol莽草酸最多能和4molNaOH中和
C. 分子中含有3种官能团
D. 在水溶液中羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
“分类”是一种思想方法,在化学发展中起到了重要作用.下列说法正确的是()
A. 氧化还原反应中,一种元素化合价升高,一定有另一种元素化合价降低
B. 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
C. 根据水溶液能否导电将化合物分为电解质和非电解质
D. 碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2S的水溶液洗患处可以用来治疗由一种小芥虫在皮肤内生活引起的皮肤病,而且用热水配制的Na2S溶液治疗效果更好.请说明原因,并写出有关的离子方程式.(已知:H2S有毒,可杀虫)
(1)可治疗的原因
(2)热水配制的原因 .
(3)离子方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com