
【题目】25℃,将浓度均为0.1mol/L的HA溶液Va mL和BOH溶液Vb mL混合,保持Va+Vb=100mL,生成物BA易溶于水。Va、Vb与混合液pH的关系如下图。下列叙述错误的是

A.HA一定是弱酸
B.BOH可能是强碱
C.z点时,水的电离被促进
D.x、y、z点时,溶液中都存在c(A-)+c(OH-)=c(B+)+c(H+)
【答案】C
【解析】
A. 当Va=Vb=50mL时,溶液相当于BA溶液,此时溶液的pH>7呈碱性,说明BA是强碱弱酸盐,这里的强弱是相对的,则HA一定是弱酸,故A正确;
B. 当Va=Vb=50mL时,溶液相当于BA溶液,此时溶液的pH>7呈碱性,说明BA是强碱弱酸盐,这里的强弱是相对的,BOH可能是强碱也可能是电离程度比HA大的弱碱,故B正确;
C. z点时,BOH溶液的体积Vb mL大于HA溶液的体积Va mL,混合溶液的pH大于9,即c(H+)<10-9,25℃时该溶液中水的电离被抑制,故C错误;
D. x、y、z点时,溶液中都存在电荷守恒:c(A-)+c(OH-)=c(B+)+c(H+),故D正确;
题目要求选择错误的,故选C。


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】无色的混合气体甲中可能含有NO、CO2、NO2、NH3、N2中的几种,将100mL气体甲经过如图所示实验处理,结果得到酸性溶液,而几乎无气体剩余,则气体甲的组成可能为( )
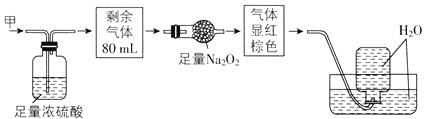
A.NO2、NH3、N2B.NH3、NO、CO2
C.NH3、NO2、CO2D.NO、CO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A为正盐,常温、常压下,B、C、D、E、G、H、I均为气体,其中D、G、H为单质,气体B能使湿润红色石蕊试纸变蓝,气体E本身为无色气体,但是与空气接触会生成一种红棕色气体I,H为黄绿色气体。F在常温下是一种无色液体。C、J的水溶液分别为两种强酸。图中反应条件(除加热外)均己略去。
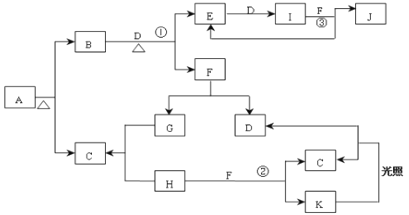
(1)写出它们的化学式:A__、C__、J__。
(2)写出②的离子反应方程式:__。
(3)写出③的化学反应方程式:__。
(4)红热的碳与J的浓溶液反应的化学方程式:__。
(5)J的浓溶液与单质Ag反应的离子方程式为:__。
(6)若86.4g银与含有1.4molJ的浓溶液恰好完全反应,则最终得到气体(NO、NO2)的总物质的量为__mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极电解饱和食盐水,下列分析错误的是
A.得电子能力H+>Na+,故阴极得到H2
B.水电离平衡右移,故阴极区得到OH-
C.失电子能力Cl->OH-,故阳极得到Cl2
D.OH-向阴极移动,故阳极区滴酚酞不变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z均为短周期主族元素,W的最外层电子数与核外电子总数之比为7:17,X与W同主族,Y的原子序数是W和X的原子序数之和的一半,含Z元素的物质在焰色反应实验中的焰色为黄色。下列判断正确的是
A.金属性:Y>ZB.非金属性:W>X
C.原子半径:W>Y>ZD.氢化物的热稳定性:X>W
查看答案和解析>>
科目:高中化学 来源: 题型:
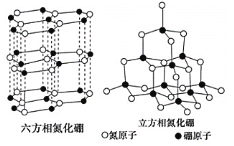
【题目】晶体硼熔点为1873K,其结构单元为正二十面体,结构如图所示。氮化硼(BN)有多种相结构,例如六方相氮化硼与立方相氮化硼,结构如图所示,六方相氮化硼与石墨相似,具有层状结构;立方相氮化硼是超硬材料。回答下列问题:
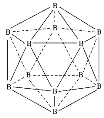
(1)基态硼原子有___种不同能量的电子,第二周期中,第一电离能介于硼元素与氮元素之间的元素有___种。
(2)晶体硼为___(填晶体类型),结构单元由___个硼原子构成,共含有___个B-B键。
(3)关于氮化硼两种晶体的说法,正确的是___。
a.立方相氮化硼含有σ键和π键
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体均为分子晶体
d.两种晶体中的B-N键均为共价键
(4)NH4BF4是合成氮化硼纳米管的原料之一,1molNH4BF4含有___mol配位键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学进行如图所示实验,以检验化学反应中的能量变化。回答下列问题
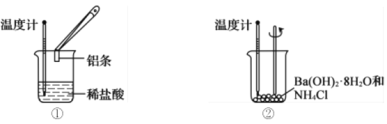
(1)装置①中反应物的总能量比生成物的总能量________(填标号)。
a.高 b.低 c.相等
(2)装置②中反应后溶液的温度__________(填标号)。
a.升高 b.降低 c.不变
(3)已知断裂1mo1共价键需要吸收的能量分别为 H —H :436kJ,I —I :151kJ,H— I :299kJ。则反应 H2+I2 = 2HI的能量变化为______(填标号)。
a.无能量变化 b.吸热 c.放热
(4)碱金属单质在空气中燃烧的产物与碱金属的活动性有关。锂单质在空气中燃烧得到的产物的化学式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
[实验目的]制取乙酸乙酯
[实验原理]甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯。
[装置设计]甲、乙、丙三位同学分别设计了下列三套实验装置:
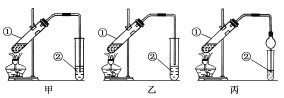
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,较合理的是________(选填“甲”或“乙”)。丙同学将甲装置中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是____________________。
[实验步骤]
Ⅰ.按丙同学选择的装置组装仪器,在试管中先加入3 mL乙醇,并在摇动下缓缓加入2 mL浓硫酸充分摇匀,冷却后再加入2 mL冰醋酸;
Ⅱ.将试管固定在铁架台上;
Ⅲ.在试管②中加入适量的饱和Na2CO3溶液;
Ⅳ.用酒精灯对试管①加热;
Ⅴ.当观察到试管②中有明显现象时停止实验。
[问题讨论]
(1)步骤Ⅰ安装好实验装置,加入样品前还应检查_____________
(2)写出试管①中发生反应的化学方程式:____________(注明反应条件)。
(3)试管②中饱和Na2CO3溶液的作用是_____________
(4)从试管②中分离出乙酸乙酯的实验操作是____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中无机氮的循环过程可用如图表示。下列说法正确的是(已知:反应④的离子方程式为4NH4+ + 5O2![]() 2NO2- + 6H+ + N2O + 5H2O)
2NO2- + 6H+ + N2O + 5H2O)

A. ①②均属于固氮反应
B. 海洋中的反硝化作用一定需要氧气参加
C. 反应④中每生成1 mol H2O转移2 mol e-
D. 向海洋排放含NO3-的废水可能影响海洋中氮的循环
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com