
| 1 |
| 2 |
| 1 |
| 2 |
| A、① | B、④ | C、②③④ | D、①②③ |


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
| A、进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| B、进行萃取操作时,应选择有机萃取剂 |
| C、进行蒸发操作时,至当出现大量固体时,应停止加热用余热蒸干 |
| D、进行分液操作时,分液漏斗中下层液体从下口放出后,换一洁净烧杯继续接取上层液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 可逆反应mX(g)+nY(g)?pZ(g),在不同的温度(T1、T2)和不同的压强(P1、P2)下,产物Z的物质的量(n)与时间(t)的关系如图所示,则下列判断正确的是( )
可逆反应mX(g)+nY(g)?pZ(g),在不同的温度(T1、T2)和不同的压强(P1、P2)下,产物Z的物质的量(n)与时间(t)的关系如图所示,则下列判断正确的是( )| A、m+n<p |
| B、m+n>p |
| C、增大压强平衡向正反应方向移动 |
| D、升高温度平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH |
| B、NaHCO3 |
| C、CH3COOK |
| D、Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入少量CH3COONa固体,平衡向正反应方向移动 |
| B、加水,反应速率变小,平衡向正反应方向移动 |
| C、滴加少量0.1mol/LHCl溶液,溶液中C(H+)减少 |
| D、加入少量NaOH固体,平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
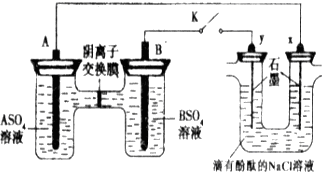
| A、A的金属活动性弱于B |
| B、Na+从y电极趋向x电极 |
| C、Y电极附近溶液先变红 |
| D、B的电极反应:B-2e-=B2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaCl、FeCl3、Na2SO4 |
| B、NaCl、FeBr3 |
| C、NaCl、Fe2O3、Na2SO4 |
| D、Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁与盐酸的反应:2Fe+6H+=2Fe3++3H2↑ |
| B、石灰石与稀盐酸反应制备二氧化碳:CO32-+2H+=H2O+CO2↑ |
| C、向氢氧化铜中滴加硫酸溶液:H++OH-=H2O |
| D、硫酸铜溶液和氢氧化钡溶液混合:Cu2++SO42-+Ba2++2OH-=Cu(OH)2↓+BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com