
����Ŀ����֪ij��ѧ��Ӧ��ƽ�ⳣ������ʽΪK=![]() ���ڲ�ͬ���¶��¸÷�Ӧ��ƽ�ⳣ�������ʾ��
���ڲ�ͬ���¶��¸÷�Ӧ��ƽ�ⳣ�������ʾ��
t/�� | 700 | 800 | 830 | 1 000 | 1 200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
�����й���������ȷ���ǣ�������
A. �÷�Ӧ�Ļ�ѧ����ʽ��CO��g��+H2O��g��![]() CO2��g��+H2��g��
CO2��g��+H2��g��
B. ������Ӧ������Ӧ�Ƿ��ȷ�Ӧ
C. ����1L���ܱ�������ͨ��CO2��H2��1mol��5min���¶����ߵ�830�棬��ʱ���CO2Ϊ0.4molʱ���÷�Ӧ�ﵽƽ��״̬
D. ��ƽ��Ũ�ȷ������й�ϵʽ��![]() �����ʱ���¶�Ϊ1000��
�����ʱ���¶�Ϊ1000��
���𰸡�C
��������
A. ƽ�ⳣ������ʽΪK=![]() ����ѧ����ʽΪCO(g)+H2O(g)
����ѧ����ʽΪCO(g)+H2O(g)![]() CO2(g)+H2(g)��A����ȷ��
CO2(g)+H2(g)��A����ȷ��
B. ƽ�ⳣ�����¶�����С��˵��ƽ��������У�����Ϊ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ��B����ȷ��
C. ����1L���ܱ�������ͨ��CO2��H2��1mol��5min���¶����ߵ�830�棬��K=1����ƽ��ʱת����CO2�����ʵ���Ϊx mol�����г�����ʽ���£�
CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
��ʼ��(mol/L)�� 1 1 0 0
ת����(mol/L)�� x x x x
ƽ����(mol/L)��1-x 1-x x x��
��K=![]() =1�����x=0.5����ƽ�����CO2�����ʵ���Ϊ0.5mol/L
=1�����x=0.5����ƽ�����CO2�����ʵ���Ϊ0.5mol/L![]() 1L=0.5mol��C�����
1L=0.5mol��C�����
D. ��ƽ��Ũ�ȷ��Ϲ�ϵ![]() ����
����![]() =0.6�����ݱ������ݿ�֪����ʱ���¶�Ϊ1000�棬D����ȷ��
=0.6�����ݱ������ݿ�֪����ʱ���¶�Ϊ1000�棬D����ȷ��
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����º��������£���˵����ӦA��s��+ 2B��g��![]() C��g��+ D��g��һ�����ڻ�ѧƽ��״̬����
C��g��+ D��g��һ�����ڻ�ѧƽ��״̬����
A. ���������ܶȲ��ٸı� B. �����ڵ�ѹǿ���ֲ���
C. C��D�����ʵ������ D. ����1 mol B��ͬʱ���� 0.5 mol D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(AlN��Al��N�����ԭ�������ֱ�Ϊ27��14)�㷺���ڵ��ӡ��մɵȹ�ҵ������һ�������£�AlN��ͨ����ӦAl2O3+N2��3C![]() 2AlN+3CO�ϳɡ�����������ȷ����(����)
2AlN+3CO�ϳɡ�����������ȷ����(����)
A.������Ӧ�У�N2�ǻ�ԭ����Al2O3��������
B.������Ӧ�У�ÿ����1mol AlN��ת��3mol����
C.AlN�е�Ԫ�صĻ��ϼ�Ϊ+3
D.AlN��Ħ������Ϊ41g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Cu��������������������������Ҫ��Ӧ�á�
I.����Cu2O���Ǻ�ĸ��ͧ�ײ��ķ���ʴͿ�ϣ�Ҳ�������Ĵ�����
��1����֪��Cu2O(s)+![]() O2(g)=2CuO(s) ��H=-196kJ/mol
O2(g)=2CuO(s) ��H=-196kJ/mol
2C(s)+O2(g)=2CO(g) ��H=-220.8kJ/mol
��ҵ����̼����CuO��ĩ�����һ�������·�Ӧ��ȡCu2O(s)��ͬʱ����CO������Ȼ�ѧ����ʽΪ___��
��2��������Cu2O��������ʵ�ּ״�������ȡ��ȩ��CH3OH(g)![]() HCHO(g)+H2(g)���״���ƽ��ת�������¶ȱ仯������ͼ��ʾ��
HCHO(g)+H2(g)���״���ƽ��ת�������¶ȱ仯������ͼ��ʾ��
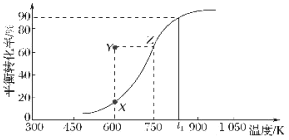
�ٸ÷�Ӧ����H___0������>������<������600Kʱ��Y��״���v������___v���棩������>������<������
����t1Kʱ����̶����Ϊ1L���ܱ������г���2molCH3OH(g)���¶ȱ��ֲ��䣬9����ʱ�ﵽƽ�⣬��0��9min����CH3OH(g)��ʾ�ķ�Ӧ����v(CH3OH)___���¶�Ϊt1ʱ���÷�Ӧ��ƽ�ⳣ��K��ֵΪ___��
II.Cu���dz����Ĵ��������dz����ĵ缫���ϡ�
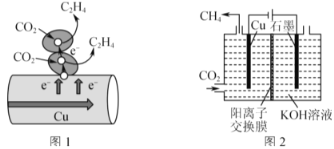
��3��ͼ1��ʾ��������CO2����ֱ�ӵ��Ӵ��ݻ��������ڴ���ͭ�ı������ת������ֱ�Ӵ��ݵĵ������ʵ���Ϊ2molʱ����μӷ�Ӧ��CO2�����ʵ���Ϊ___��
��4��ͼ2��ʾ��KOH��Һ���������Һ���е���ʾ��ͼ��CO2��Cu�缫�Ͽ���ת��ΪCH4���õ缫��Ӧ�ķ���ʽΪ___��
III.��ͭ���ӵķ�ˮ�������Ⱦ��ͨ������ת��Ϊ��ͭ��������ȥ��
��5����֪��Ksp(CuS)=1��10-36��Ҫʹͭ���ӵ�Ũ�ȷ����ŷű���������0.4mg/L������Һ�е������ӵ����ʵ���Ũ������Ϊ___mol/L��������С�����һλ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ij������N2��H2��Ӧ�����������仯������ͼ������ͼ���ж�������������ȷ���ǣ�������
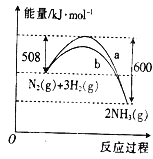
A. �÷�Ӧ���Ȼ�ѧ����ʽΪN2��g��+3H2��g��![]() 2NH3��g�� ��H=+92kJ��mol��1
2NH3��g�� ��H=+92kJ��mol��1
B. a�����Ǽ������ʱ�������仯����
C. ����������û�ѧ��Ӧ�ķ�Ӧ����ֵ���С
D. ��Ӧ2NH3��g��![]() N2��g��+3H2��g����H=+92kJ��mol��1
N2��g��+3H2��g����H=+92kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��﮺�ˮ��س����ں��ϸ���������豸�У���ʾ��ͼ��ͼ��ʾ����ط�ӦΪ2Li��2H2O===2LiOH��H2������ع���ʱ������˵����������( )

A. �����������
B. ���Ӵ�﮵缫�������������缫
C. �ɽ�����ת��Ϊ��ѧ��
D. ��ˮ��Ϊ�������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ����ʵ����ƽ���ƶ�ԭ�����͵��ǣ�������
A. ��ӦI2��g��+H2��g��![]() 2HI��g�� ��ƽ���ѹ�������ϵ��ɫ����
2HI��g�� ��ƽ���ѹ�������ϵ��ɫ����
B. H2O2�м���������̣��������������ʼӿ�
C. �ػ�ɫ��FeCl3��Һ�м���������ɫ��Ϊdz��ɫ
D. ��ӦCO��g��+NO2��g��![]() CO2��g��+NO��g����H��0����ƽ��������¶���ϵ��ɫ����
CO2��g��+NO��g����H��0����ƽ��������¶���ϵ��ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һˮ�����İ���ͭ����[Cu(NH3)4SO4��H2O����Է�������Ϊ246]��һ����Ҫ��Ⱦ�ϼ�ũҩ�м��塣�����¸����ʿ�����ˮ���������Ҵ���ij��ѧ��ȤС��ͨ������ʵ���Ʊ�һˮ�����İ���ͭ���岢�ⶨ�䴿�ȡ��ش�������⣺
I��ʵ������ȡCuSO4��Һ
����i��ͭ��Ũ��������Ʊ���
����ii����ͭ���ڿ����г�ּ�������ȫ��ڣ��ټ�ϡ���ἴ�ɵõ�����ͭ��Һ��
(1)��д������i��Ӧ�Ļ�ѧ����ʽ____����ȱ����____��д1�㣩��
(2)ʵ�������з���ii�������Ϻ�ɫ����δ��Ӧ������ԭ�������____��
(3)���ڴˣ�ʵ������˸Ľ�������һ�ַ������������ͭ�ķ�Ӧ�����еμ�H2O2��Һ���۲쵽��������____��д1�㣩��H2O2�ķе�Ϊ150.2�档Ϊ�ӿ췴Ӧ��Ҫ���H2O2��Һ��Ũ�ȣ���ͨ����ͼ��H2O2ϡ��ҺŨ������ˮ�����____����a��b�������Ӽ�ѹ�豸��Ŀ����____��
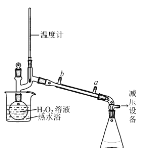
II��һˮ�����İ���ͭ������Ʊ�
(4)����ͭ��Һ����һ�������ᣬ�����ԣ���������NH3��H2O������ҺpH������dz��ɫ��������֪��ɷ�ΪCu2(OH)2SO4����д�����ɴ˳��������ӷ�Ӧ����ʽ__________��
(5)�����μ�NH3��H2O����ת��������ɫ��Һ��������ɫ��Һ����������ɫ����ļ��ʵ���ǵμ�____________��
III����Ʒ���ȵIJⶨ
(6)��ȷ��ȡmg���壬������ˮ�ܽ⣬Ȼ����μ�������NaOH��Һ��ͨ��ˮ��������ȫ����������V1mL0.200mol��L��1��������ȫ���ա��Լ�����ָʾ������0.200mol��L��1NaOH����Һ�ζ���ʣ��HCl�����յ�ʱ����V2mLNaOH��Һ����Ʒ���ȵı���ʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£��ܱ������з�����ӦaX(g) ![]() bY(g)��cZ(g)���ﵽƽ������¶Ȳ��䣬���������ݻ�ѹ����ԭ���ݻ���һ�룬���ﵽ��ƽ��ʱ������Y��Z��Ũ�Ⱦ���ԭ����1.8����������������ȷ����
bY(g)��cZ(g)���ﵽƽ������¶Ȳ��䣬���������ݻ�ѹ����ԭ���ݻ���һ�룬���ﵽ��ƽ��ʱ������Y��Z��Ũ�Ⱦ���ԭ����1.8����������������ȷ����
A. ���淴Ӧ�Ļ�ѧ��������a��b��c
B. �ﵽ��ƽ��ʱ������X��ת���ʼ�С
C. ѹ���������ݻ�ʱ���������������С
D. �ﵽ��ƽ��ʱ���������Z��������������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com