
| A. | 晶体中不一定存在分子间作用力,但一定存在化学键 | |
| B. | 液态氟化氢中存在氢键,所以其沸点比氯化氢更高 | |
| C. | 向Fe(NO3)2溶液中通入过量的HI,最终Fe2+全部氧化成Fe3+ | |
| D. | 普通玻璃是将石灰石、石英、黏土在玻璃熔炉中高温熔融制得的 |
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:选择题

| A. | 两种物质的分子式均为C10H14O2互为同分异构体 | |
| B. | 两种物质均能发生加成和取代反应 | |
| C. | 两种物质都有甲基、苯环和羧基 | |
| D. | 两物质都含有双键因此都能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅的化学性质不活泼,能与强碱反应不与任何酸反应 | |
| B. | 生物炼铜就是利用植物对铜离子的吸收达到富集铜的目的 | |
| C. | 过量二氧化硫通入石蕊溶液中能使石蕊溶液先变红色后褪色 | |
| D. | 工业上利用氢气在氯气中燃烧生成氯化氢,再将氯化氢溶于水制得盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ar原子的结构示意图: | |
| B. | 丙烷分子的比例模型: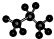 | |
| C. | NaClO的电子式: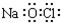 | |
| D. | HCO3-电离方程式:HCO3-+H2O?CO32-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径大小:Z>Y | |
| B. | Z和Y、W都能形成A2B2型的化合物 | |
| C. | Y和W形成的氢化物的稳定性:W>Y | |
| D. | X、Y、Z、W四种元素形成的化合物水溶液一定显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有等物质的量的氢氧化钡、明矾两种溶液混合:3Ba2++6OH-+2Al3++3SO42-═3BaSO4+2Al(OH)3↓ | |
| B. | 纯碱溶液与胆矾溶液混合生成正盐、酸式盐、碱式盐:3CO32-+2Cu2++2H2O═2HCO3-+Cu2(OH)2CO3↓ | |
| C. | H218O中投入Na2O2固体:2H218O+2O22-═4OH-+18O2↑ | |
| D. | 0.1mol•L-1CuCl2溶液中加入0.1mol•L-1NaHS溶液:Cu2++HS-═CuS↓+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com