
常温下,0.2mol·L-1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
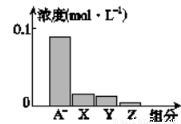
A.HA为强酸
B.该混合液pH=7
C.图中X表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y)=c(Na+)
科目:高中化学 来源:2016-2017学年河南省高一上第一次考试化学卷(解析版) 题型:选择题
有机物苯酚的试剂瓶上有如图标识,此标识的含义是
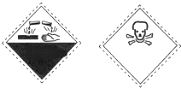
A. 自燃物品、易燃 B. 腐蚀品、有毒
C. 爆炸品、腐蚀性 D. 氧化剂、有毒
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上10月月考化学试卷(解析版) 题型:选择题
下列实验操作、现象与实验结论一致的是( )
选项 | 实验操作及现象 | 实验结论 |
A | SO2通入Ba(NO3)2溶液中,有白色沉淀生成 | 发生复分解反应生成难溶物质BaSO3 |
B | 某溶液滴加盐酸酸化的BaCl2溶液,生成白色沉淀 | 该溶液中可能不含SO42- |
C | 将FeCl3溶液分别滴入NaBr、NaI溶液中,再分别 滴加CCl4,振荡,静置,下层分别呈无色和紫红色 | 氧化性:Fe3+﹥Br2﹥I2 |
D | 向浓度均为0.1 mol·L-1的KCl、KI混合溶液中滴 加1~2滴0.01 mol·L-1 AgNO3溶液,沉淀呈黄色 | Ksp(AgCl)﹤Ksp(AgI) |
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上10.6周测化学试卷(解析版) 题型:选择题
25℃时纯水的电离度为a1,pH=2的醋酸溶液中水的电离度为a2,pH=12的氢氧化钠溶液中水的电离度为a3。若将上述醋酸与氢氧化钠溶液等体积混合,所得溶液中水的电离度为a4。下列关系式中正确的是
A.a2 = a3<a4<a1 B.a3 = a2<a1<a4
C.a2<a3<a1<a4 D.a1<a2<a3<a4
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上10.6周测化学试卷(解析版) 题型:选择题
常温下已知两种一元弱酸HX和HY,如果向NaX溶液中通入CO2气体,只能生成HX和NaHCO3;向NaY溶液中通入CO2,只生成HY和Na2CO3,下列有关叙述正确的是
A.酸性由强到弱:H2CO3>HX>HY
B.结合质子能力:CO32->Y->X->HCO3-
C.溶液酸性:NaX>Na2CO3>NaY>NaHCO3
D.向NaX溶液中通入足量CO2后的离子浓度:c(X-)>c(Na+)>c(HCO3-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上10.6周测化学试卷(解析版) 题型:选择题
把0.05molNaOH固体分别加入到100mL下列液体中,溶液导电能力变化最小的是
A.自来水 B.0.5mol/L盐酸
C.0.5mol/LHAc溶液 D.0.5mol/LKCl溶液
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上学期第一次月考化学卷(解析版) 题型:选择题
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6mol•L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2 2.4L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
2.4L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
A.上述电解过程中共转移2 mol电子
B.原混合溶液中c(K+)为2 mol·L-1
C.电解得到的Cu的物质的量为0.5 mol
D.电解后溶液中c(H+)为2 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月月考化学卷(解析版) 题型:填空题
已知H2、CO、CH4的燃烧热分别为ΔH1=-285.8 kJ/mol、ΔH2=-283 kJ/mol、ΔH3=-890 kJ/mol。H2O(g)=H2O(l) ΔH4=-44 kJ/mol。回答下列问题:
(1)用CH4替代水煤气作家用燃气的优点是____________________。将煤气灶改为天然气灶时,应适当调_________(填“大”或“小”)空气进气阀门。
(2)合成氨厂一般采用烃(以CH4为例)和水蒸气反应制取原料气H2,发生如下反应:CH4(g)+H2O(g)  CO(g)+3H2(g)。
CO(g)+3H2(g)。
①该反应的ΔH=________________。
②当该反应达到平衡状态时,下列说法一定正确的是__________(填字母)。
A.v(CH4)=v(CO) B.加入催化剂,ΔH不变
C.升高温度,平衡常数K增大 D.CH4与H2O的转化率相等
③T℃时,该反应的初始浓度与起始速率的部分数据如下:
初始浓度/mol·L-1 | 起始速率/mol3·L-3·s-1 | |
c(CH4) | c(H2O) | v |
0.10 | 0.10 | 1.0×10-4 |
0.10 | 0.20 | 4.0×10-4 |
0.30 | 0.20 | 1.2×10-3 |
写出起始速率与初始浓度的关系式[用c(CH4)、c(H2O)及适当的速率常数表示]v=________。
④T℃时,在一个体积可变的恒压密闭容器中,充入0.1 mol CH4、0.1 mol H2O(g)发生反应,起始时容器的体积为1 L。CH4的转化率与反应时间的关系如图中曲线A所示。则T℃时该反应的平衡常数K=____________。若温度与投料方式相同,该反应在容积为1 L的恒容密闭容器中进行,刚达平衡状态的点是__________(选填B、C、D、E)。

查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上第一次月考化学卷(解析版) 题型:填空题
2014年8月28日,第二届夏季青年奥林匹克运动会(以下简称“青奥会”)在南京奥体中心顺利闭幕。请完成下列与“青奥会”有关的填空。
(1)随着“青奥会”的举行,各种与城市建设相关的新材料接连不断地展现出。
①体育场馆需用大量的建筑材料。下列材料不属于硅酸盐材料的是 (填字母)。
a.石灰石 b.水泥 c.玻璃
②轨道交通建设需大量金属材料。下列金属材料最易发生腐蚀的是 (填字母)。
a.铝合金 b.钢铁 c.纯铜
(2)“青奥会”期间,要保障运动员的营养与健康。
①及时补充体能是运动员取得优秀成绩的基本保证。氨基酸是组成蛋白质的基本单元,其分子中所含官能团是 (填名称)和 (填名称);脂肪在人体内水解的产物是高级脂肪酸和 (填名称)。
②运动员还要合理吸收维生素。维生素C的结构简式如图 所示,其分子式为 ;在氯化铁溶液中加入维生素C后,溶液由黄色转变为浅绿色,说明维生素C具有较强的 性(填“氧化”或“还原”)
所示,其分子式为 ;在氯化铁溶液中加入维生素C后,溶液由黄色转变为浅绿色,说明维生素C具有较强的 性(填“氧化”或“还原”) 。
。

③服用 违禁药物不仅妨碍体育竞技的公平、公正,也有害运动员的身心健康。在阿司匹林、青霉素、麻黄碱、小苏打等常用药物中,参赛选手不可服用的是 。
违禁药物不仅妨碍体育竞技的公平、公正,也有害运动员的身心健康。在阿司匹林、青霉素、麻黄碱、小苏打等常用药物中,参赛选手不可服用的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com