
| A. | 该浓硝酸中HNO3的物质的量浓度是14.0mol/L | |
| B. | 加入NaOH溶液的体积是50mL | |
| C. | 浓硝酸在与合金反应中起了酸性和氧化性的双重作用 | |
| D. | 得到的金属氢氧化物的沉淀为3.12克 |
分析 A.根据c=$\frac{1000ρw}{M}$计算该浓硝酸的物质的量浓度;
B.加入适量的1.0mol/L NaOH溶液,恰使溶液中的金属离子全部沉淀,此时溶液中溶质为NaNO3,由N元素守恒可知n(NaNO3)+n(NO2)=n(HNO3),由钠离子守恒n(NaOH)=n(NaNO3),再根据V=$\frac{n}{c}$计算;
C.起氧化性的硝酸生成NO2气体,起酸性的硝酸生成硝酸根;
D.由电荷守恒可知,氢氧化物中氢氧根的物质的量等于转移电子物质的量,根据二氧化氮计算转移电子物质的量,氢氧化物质量等于金属质量与氢氧根质量之和.
解答 解:A.密度为1.40g/cm3、质量分数为63%的浓硝酸的物质的量浓度=$\frac{1000×1.4×63%}{63g/mol}$mol/L=14mol/L,故A正确;
B.加入适量的1.0mol/L NaOH溶液,恰使溶液中的金属离子全部沉淀,此时溶液中溶质为NaNO3,由N元素守恒可知n(NaNO3)+n(NO2)=n(HNO3),则n(NaNO3)=0.05L×14mol/L-$\frac{1.792L}{22.4L/mol}$=0.62mol,由钠离子守恒n(NaOH)=n(NaNO3)=0.62mol,故需要1.0mol/L NaOH溶液体积为$\frac{0.62mol}{1mol/L}$=0.62L=620mL,故B错误;
C.起氧化性的硝酸生成NO2气体,起酸性的硝酸生成硝酸根,所以浓硝酸在与合金反应中起了酸性和氧化性的双重作用,故C正确;
D.由电荷守恒可知,氢氧化物中氢氧根的物质的量等于转移电子物质的量,即氢氧根的物质的量为0.08mol×(5-4)=0.08mol,故氢氧化物质量=1.76g+0.08mol×17g/mol=3.12g,故D正确,
故选B.
点评 本题考查混合物的有关计算,难度中等,理解反应发生的过程是关键,是对学生综合能力的考查,注意根据守恒思想进行的解答.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 136.8kJ | B. | 110.9kJ | C. | 83.2kJ | D. | 82.4kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | Y | |
| Z | W |
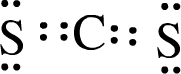 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
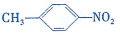 和
和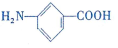
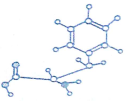
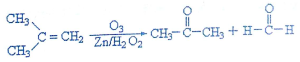

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与浓硫酸、浓硝酸共热并保持55~60℃反应生成硝基苯 | |
| B. | 甲苯与氯气在光照的条件下反应主要生成2,4-二氯甲苯 | |
| C. | 苯酚与浓溴水反应生成2,4,6-三溴苯酚 | |
| D. | 丙烯与溴的四氯化碳溶液反应生成1,2-二溴丙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 成分 | 质量(g) | 摩尔质量(mol•L-1) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
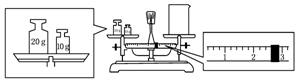
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
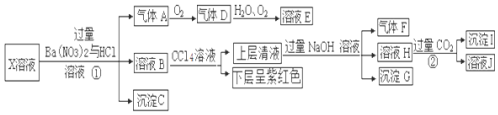
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:F2>Cl2 | B. | 碱性:Mg(OH)2>Al(OH)3 | ||
| C. | 金属单质置换出氢的能力:K>Na | D. | 酸性:H2SO4>HClO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com