
| A. | 甲苯和硝酸反应生成三硝基甲苯 | |
| B. | 甲苯能使酸性高锰酸钾溶液褪色 | |
| C. | 1mol甲苯能与3mol氢气发生加成反应 | |
| D. | 甲苯可以燃烧并产生浓烈的黑烟 |
分析 A.甲苯和苯都能发生取代反应;
B.苯、甲烷不能被酸性KMnO4溶液氧化,甲苯能被酸性KMnO4溶液氧化为苯甲酸;
C.苯也能与氢气发生加成反应;
D.燃烧产生带浓烟的火焰说明含碳量高,不完全燃烧.
解答 解:A.甲苯和苯都能与浓硝酸、浓硫酸发生取代反应,所以不能说明苯环对侧链有影响,故A错误;
B.甲苯可看作是CH4中的1个H原子被-C6H5取代,苯、甲烷不能被酸性KMnO4溶液氧化使其褪色,甲苯能被酸性KMnO4溶液氧化为苯甲酸,苯环未变化,侧链甲基被氧化为羧基,说明苯环影响甲基的性质,故B正确;
C.苯、甲苯都能能与H2发生加成反应,是苯环体现的性质,不能说明苯环对侧链性质产生影响,故C错误;
D.燃烧产生带浓烟的火焰说明含碳量高,不能说明苯环对侧链性质产生影响,故D错误,
故选B.
点评 本题以苯及其同系物的性质考查为载体,旨在考查苯的同系物中苯环与侧链的相互影响,通过实验性质判断,考查学生的分析归纳能力.


科目:高中化学 来源: 题型:解答题
 ,F元素离子基态时的电子排布式1s22s22p63s23p6,E元素的原子结构示意图是
,F元素离子基态时的电子排布式1s22s22p63s23p6,E元素的原子结构示意图是 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④⑤ | C. | ①②④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol | B. | 1mol | C. | 2.25 mol | D. | 2.5 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入有色布条,有色布条褪色,说明溶液中有氯气分子存在 | |
| B. | 溶液呈现黄绿色,且有刺激性气味,说明有氯气分子存在 | |
| C. | 先加入盐酸酸化,再加入硝酸银溶液产生白色沉淀,说明有Cl-存在 | |
| D. | 加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤⑦ | B. | ②③⑥ | C. | ②④ | D. | ②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阳极反应为Fe-2e-═Fe2+ | |
| B. | 过程中有Fe(OH)3沉淀生成 | |
| C. | 电路中每转移12mol电子,最多有1molCr2O72-被还原 | |
| D. | 如果石墨做阴阳极,电解过程不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
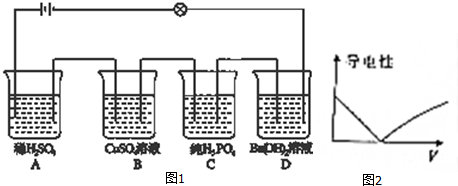
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com