
| 选项 | M | N | 除杂试剂 | 除杂方法 |
| A | C2H5OH | H2O | 生石灰 | 蒸馏 |
| B | CH4 | CH2═CH2 | 酸性KMnO4溶液 | 洗气 |
| C | CH3COOCH2CH3 | CH3COOH、C2H5OH | NaOH溶液 | 分液 |
| D | 苯酚 | 三溴苯酚 | 水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.生石灰吸收水,利于乙醇的蒸馏;
B.乙烯被氧化生成二氧化碳气体;
C.乙酸乙酯、乙酸都与氢氧化钠溶液反应;
D.苯酚、三溴苯酚互溶.
解答 解:A.生石灰吸收水,可增大沸点差,利于乙醇的蒸馏,可用于除杂,故A正确;
B.乙烯被氧化生成二氧化碳气体,引入新杂质,应用溴水除杂,故B错误;
C.乙酸乙酯、乙酸都与氢氧化钠溶液反应,应加入饱和碳酸钠溶液除杂,故C错误;
D.苯酚、三溴苯酚互溶,用过滤的方法不能分离,可用蒸馏的方法分离,故A正确.
故选A.
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析、实验能力的考查,注意把握物质的性质的异同,把握实验的严密性和可行性的评价,注意除杂时不能引入新杂质,更不能影响被提纯的物质,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2、NaClO中所含化学键类型完全相同 | |
| B. | 只有活泼金属与活泼非金属元素之间才能形成离子键 | |
| C. | D2O和T2O是同一物质 | |
| D. | 氯气与NaOH反应的过程中,同时又离子键、极性键和非极性键的断裂和形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
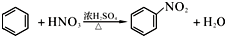
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 10gH2和10gO2 | B. | 5.6LN2(标准状况)和11gCO2 | ||
| C. | 9gH2O和0.5molBr2 | D. | 22.4mLH2(标准状况)和0.1molN2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
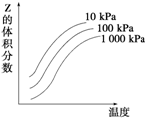 下图是温度和压强对可逆反应 X+Y?2Z 反应影响的示意图.图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数.下列叙述正确的是( )
下图是温度和压强对可逆反应 X+Y?2Z 反应影响的示意图.图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数.下列叙述正确的是( )| A. | 上述可逆反应的正反应为放热反应 | B. | X、Y、Z均为气态 | ||
| C. | X和Y状态无法确定,Z为气态 | D. | 上述反应的逆反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴加KI溶液时,转移2 mol e-时生成 1 mol白色沉淀 | |
| B. | 通入SO2后溶液逐渐变成无色,不是 SO2的漂白性 | |
| C. | 通入SO2时,SO2与I2反应,I2作氧化剂 | |
| D. | 上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com