

| 催化剂 |
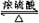 CH3COOC2H5+H2O;
CH3COOC2H5+H2O; ,
,| 催化剂 |
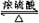 CH3COOC2H5+H2O;
CH3COOC2H5+H2O; .
.


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:
| A、O、Cl、S、P |
| B、K+、Mg2+、Al3+、H+ |
| C、I-、Br-、Cl-、S2- |
| D、Al3+、Mg2+、Ca2+、Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
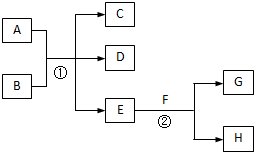 在下列各变化中,E为无色无味的液体(常温下),F为淡黄色粉末,G为常见的无色气体(反应条件均已省略).
在下列各变化中,E为无色无味的液体(常温下),F为淡黄色粉末,G为常见的无色气体(反应条件均已省略).查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、氧化剂是MnO2,还原剂是HCl |
| B、每生成1mol Cl2,转移电子的物质的量为2mol |
| C、每消耗1mol MnO2,起还原剂作用的HCl消耗4mol |
| D、转移电子的物质的量为1mol时,生成标准状况下Cl2的体积为11.2L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com