
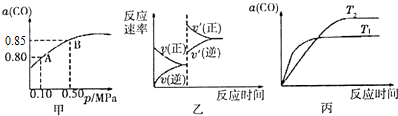
| A、由图甲知,A点CO的平衡浓度为0.4 mol?L-1 |
| B、由图甲知,B点CO、O2、CO2的平衡浓度之比为2:l:2 |
| C、达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示 |
| D、若0.50 MPa时不同温度下CO转化率与温度关系如丙图,则T2>T1 |
| 0.4mol |
| 10L |


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
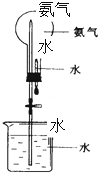 哈伯因为氨气的合成曾获1918年诺贝尔奖.
哈伯因为氨气的合成曾获1918年诺贝尔奖.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol/L |
| B、pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 |
| C、pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-) |
| D、pH相同的①CH3COONa、②NaHCO3两种溶液的c(Na+):①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
| B、充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O |
| C、放电时每转移3mol电子,正极有1mol K2FeO4被还原 |
| D、放电时正极附近溶液的酸性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
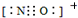
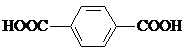 )、4,4′-联吡啶
)、4,4′-联吡啶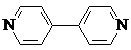 (可简化为
(可简化为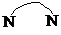 )等与Ni2+能形成多核配合物.配合物[Ni2(TPHA)(bpy)4](ClO4)2络离子的结构如图2:
)等与Ni2+能形成多核配合物.配合物[Ni2(TPHA)(bpy)4](ClO4)2络离子的结构如图2: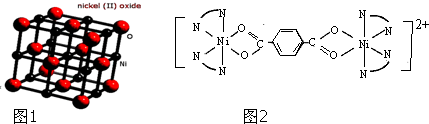
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.68 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4 L H2和O2的混合气体中所含的分子数为NA |
| B、6.8g熔融的KHSO4中含有0.05NA个阳离子 |
| C、21.6 g X单质与Cl2完全反应,生成106.8 g XC13.,则X的相对原子质量为27g/mol |
| D、0.1molNa2O2晶体中含有0.1NA个阴离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com