
| A. | 20mL 0.1mol/L CH3COONa溶液与10mL 0.1mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| B. | 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) | |
| D. | 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
分析 A.20mL 0.1mol/L CH3COONa溶液与10mL 0.1mol/L HCl溶液混合后发生反应,CH3COONa+HCl=NaCl+CH3COOH,反应后溶液为等浓度的CH3COONa和CH3COOH的混合溶液,溶液显呈酸性,醋酸电离大于醋酸根离子水解;
B.0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合反应,NaHCO3+NaOH=Na2CO3+H2O,得到碳酸钠溶液,比较碳酸钠溶液中离子浓度大小;
C.pH=12的氨水与pH=2的盐酸中,氨水浓度大于盐酸,等体积混合,氨水过量,溶液呈碱性,结合溶液中电荷守恒分析判断;
D.0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合得到醋酸钠溶液,溶液中存在质子守恒;
解答 解:A.20mL 0.1mol/L CH3COONa溶液与10mL 0.1mol/L HCl溶液混合后发生反应,CH3COONa+HCl=NaCl+CH3COOH,反应后溶液为等浓度的CH3COONa、NaCl和CH3COOH的混合溶液,溶液显呈酸性,醋酸电离大于醋酸根离子水解,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+),故A正确;
B.0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合反应,NaHCO3+NaOH=Na2CO3+H2O,得到碳酸钠溶液,碳酸根离子分步水解溶液显碱性,比较碳酸钠溶液中离子浓度大小,c(Na+)>c(CO32-)>c(OH-)>c(HCO3-),故B错误;
C.pH=12的氨水与pH=2的盐酸中,氨水浓度大于盐酸,等体积混合,氨水过量,溶液呈碱性,c(OH-)>c(H+),结合溶液中电荷守恒分析,c(H+)+c(NH4+)=c(OH-)+c(Cl-),c(NH4+)>c(Cl-),c(Cl-)+c(H+)<c(NH4+)+c(OH-),故C错误;
D.0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合得到醋酸钠溶液,溶液中存在质子守恒,所得溶液中:c(OH-)=c(H+)+c(CH3COOH),故D错误;
故选A.
点评 本题考查了弱电解质的电离、酸碱混合溶液定性判断等知识点,根据酸碱混合溶液的酸碱性结合电荷守恒来分析解答,注意电解质电离平衡的存在,题目难度中等.


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
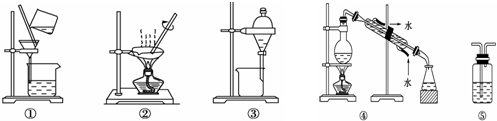
| A. | 分离Na2CO3溶液和苯,选④ | B. | 用CCl4提取碘水中的碘,选③ | ||
| C. | 用FeCl2溶液吸收Cl2,选⑤ | D. | 粗盐提纯,选①和② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铜与盐酸反应:H++OH-═H2O | |
| B. | 铝粉与氢氧化钠溶液反应:Al+2OH-═AlO2-+H2↑ | |
| C. | 利用腐蚀法制作印刷电路板:Fe3++Cu═Fe2++Cu2+ | |
| D. | 在氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ①② | C. | ①③ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S$→_{燃烧}^{O_{2}}$SO2$\stackrel{BaCl_{2}(aq)}{→}$BaSO4 | |
| B. | SiO2$\stackrel{H_{2}O}{→}$H2SiO3$\stackrel{NaOH(aq)}{→}$Na2SiO3(aq) | |
| C. | MgCl2•6H2O$\stackrel{△}{→}$MgCl2$\stackrel{通电}{→}$Mg | |
| D. | CuSO4(aq)$\stackrel{过量NaOH(aq)}{→}$Cu(OH)2悬浊液$→_{△}^{葡萄糖}$Cu2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -488.3 kJ/mol | B. | -244.15 kJ/mol | C. | 488.3 kJ/mol | D. | 244.15 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
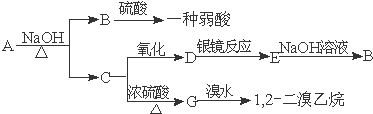
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com