
 ,F元素原子的电子排布式1s22s22p63s23p5,E元素的原子结构示意图是
,F元素原子的电子排布式1s22s22p63s23p5,E元素的原子结构示意图是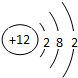
分析 A、B、C、D、E、F为六种短周期元素,它们核电荷数依次递增.B原子核外最外层电子数是次外层电子数的两倍,原子只能有2个电子层,最外层电子数为4,故B为碳元素;B原子电子总数是E原子总数的$\frac{1}{2}$,则E原子核外电子数为12,故E为Mg;由原子序数可知,F处于第三周期,F是同周期元素中原子半径最小的元素,故F为Cl;D2-与E2+的电子层结构相同,离子核外电子数为10,故D为O元素;C的原子序数介于碳、氧之间,故C为N元素;B与D可以形成三原子化合物甲为CO2;A是非金属元素,且A、C、F可形成离子化合物乙,则A为H元素,乙为NH4NO3,据此解答.
解答 解:A、B、C、D、E、F为六种短周期元素,它们核电荷数依次递增.B原子核外最外层电子数是次外层电子数的两倍,原子只能有2个电子层,最外层电子数为4,故B为碳元素;B原子电子总数是E原子总数的$\frac{1}{2}$,则E原子核外电子数为12,故E为Mg;由原子序数可知,F处于第三周期,F是同周期元素中原子半径最小的元素,故F为Cl;D2-与E2+的电子层结构相同,离子核外电子数为10,故D为O元素;C的原子序数介于碳、氧之间,故C为N元素;B与D可以形成三原子化合物甲为CO2;A是非金属元素,且A、C、F可形成离子化合物乙,则A为H元素,乙为NH4NO3.
(1)C单质为N2,分子中N原子之间形成3对共用电子对,电子式为 ,F为Cl元素,原子的电子排布式为1s22s22p63s23p5,E为Mg元素,原子结构示意图是
,F为Cl元素,原子的电子排布式为1s22s22p63s23p5,E为Mg元素,原子结构示意图是 ,
,
故答案为: ;1s22s22p63s23p5;
;1s22s22p63s23p5; ;
;
(2)化合物乙为NH4NO3,含有的化学键有:离子键、共价键、配位键,故答案为:离子键、共价键、配位键;
(3)化合物甲为CO2,固体时属于分子晶体,Mg在二氧化碳燃烧生成MgO与碳,反应方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,
故答案为:分子;2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,侧重对化学用语的考查,有利于基础知识的巩固.


科目:高中化学 来源: 题型:解答题
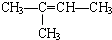 不属于烃类的是④(填序号,下同),与①互为同系物的是②,与③互为同分异构体的是⑤.
不属于烃类的是④(填序号,下同),与①互为同系物的是②,与③互为同分异构体的是⑤.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ②③⑤ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
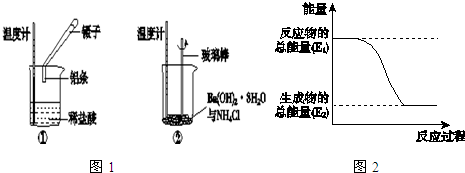
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数为34 | B. | 氢化物比HBr稳定 | ||
| C. | 非金属性比硫强 | D. | 最高价氧化物的水化物显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
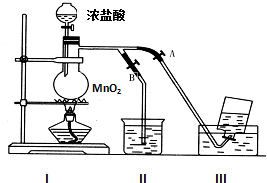 如图表示在没有通风橱收集纯净的氯气时设计的装置,图中A、B是可控制的弹簧铁夹.
如图表示在没有通风橱收集纯净的氯气时设计的装置,图中A、B是可控制的弹簧铁夹.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素 | Al | B | Be | C | Cl | X | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | Mg | N | Y | O | P | S | Si |
| 电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com