
【题目】NA为阿伏加德罗常数,下列说法正确的是
A. 28g乙烯所含共用电子对数目为2NA
B. 14g乙烯、丙烯、丁烯的混合气体中,所含原子数为3NA
C. 标准状况下,11.2L氟化氢所含分子数为0.5NA
D. 1.5g甲基所含电子数为NA
科目:高中化学 来源: 题型:
【题目】(1)同温同压下,同体积的甲烷(CH4)和二氧化碳物质的量之比为__________,原子总数之比为__________,密度之比为__________。
(2)在标准状况下,4 g H2、11.2 L O2、1 mol H2O中,所含分子数最多的是__________,质量最大的是__________,体积最小的是__________。
(3)标况下,1.92 g 某气体的体积为 672 mL,则此气体的相对分子质量为_____。
(4)已知某硫酸溶液的密度为 1.84 g/cm3,质量分数为 98%,则该硫酸的物质的量浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组研究了铜片与![]() 反应的速率,实现现象记录如下表。
反应的速率,实现现象记录如下表。
实验 | 时间段 | 现象 |
|
| 铜片表面出现极少气泡 |
| 铜片表面产生较多气泡,溶液呈很浅的蓝色 | |
| 铜片表面均匀冒出大量气泡 | |
| 铜片表面产生较少气泡,溶液蓝色明显变深,液面上方呈浅棕色 |
为探究影响该反应速率的主要因素,小组进行如下实验。
实验I:监测上述反应过程中溶液温度的变化,所得曲线如下图。
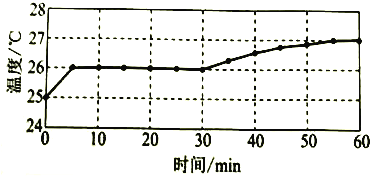
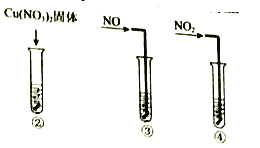
实验II:②-④试管中加入大小、形状相同的铜片和相同体积、 ![]() 。结果显示:
。结果显示:![]() 对
对![]() 和
和![]() 反应速率的影响均不明显,
反应速率的影响均不明显,![]() 能明显加快该反应的速率。
能明显加快该反应的速率。
实验III:在试管中加入铜片和![]() ,当产生气泡较快时,取少量反应液于试管中,检验后发现其中含有
,当产生气泡较快时,取少量反应液于试管中,检验后发现其中含有![]() 。
。
(1)根据表格中的现象,描述该反应的速率随时间的变化情况:____________。
(2)实验![]() 的结论:温度升高___________(填“是”或“不是”)反应速率加快的主要原因。
的结论:温度升高___________(填“是”或“不是”)反应速率加快的主要原因。
(3)实验II的目的是:__________
(4)小组同学查阅资料后推测:该反应由于生成某中间产物而加快了反应速率。请结合实验II、III,在下图方框内填入相应的微粒符号①____②_____,以补全催化机理。
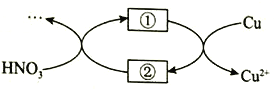
(5)为验证(4)中猜想,还需补充一个实验:__________(请写出操作和现象)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比法是常见的研究物质性质的方法之一,可用来预测很多物质的性质,但类比是相对的,必须遵循客观实际,下列说法中正确的是( )
A. ![]() 通入
通入![]() 溶液中没有现象,
溶液中没有现象,![]() 通入
通入![]() 溶液中也无明显现象
溶液中也无明显现象
B. ![]() 与
与![]() 会因为水解相互促进而完全反应生成
会因为水解相互促进而完全反应生成![]() 和
和![]() ,
,![]() 与
与![]() 也可以水解相互促进至完全反应生成
也可以水解相互促进至完全反应生成![]() 和
和![]()
C. 偏铝酸是一元酸,因此,![]() 也是一元酸
也是一元酸
D. ![]() 在标准状况下为气体,所以
在标准状况下为气体,所以![]() 在标准状况下同样为气体
在标准状况下同样为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是化工合成中最重要的镍源,在实验室中模拟工业上利用金属镍废料(含镍、铁、铝)生产氯化镍晶体
是化工合成中最重要的镍源,在实验室中模拟工业上利用金属镍废料(含镍、铁、铝)生产氯化镍晶体![]() 流程如下:
流程如下:

下表列出了相关金属离子生产氢氧化物沉淀的pH:
氢氧化物 |
|
|
|
|
开始沉淀的pH | 7.6 | 2.7 | 7.1 | 3.7 |
沉淀完全的pH | 9.6 | 3.7 | 9.2 | 4.7 |
回答下列问题:
(1)加入![]() 氧化时发生反应的离子方程式为________________________,调pH的范围为____________,若调
氧化时发生反应的离子方程式为________________________,调pH的范围为____________,若调![]() ,则溶液中
,则溶液中![]() _______________。(已知
_______________。(已知![]() ,
,![]() )
)
(2)滤液A的溶质主要是______________________。
(3)操作①的实验方法依次是_____________、_____________、过滤、洗涤、干燥,操作②的实验方法是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中水只作还原剂的是
A.2H2O+2Na=2NaOH+H2↑
B.H2O + 3NO2 = 2HNO3 + NO
C.2H2O + 2F2 = O2 + 4HF
D.3H2O (沸水) + FeCl3![]() Fe (OH)3(胶体) + 3HCl
Fe (OH)3(胶体) + 3HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常情况下,pH<7 的溶液显酸性,pH=7 的溶液显中性,pH>7 的溶液显碱性。以 FeCl3 溶液为实验对象,探究其与碱性物质之间反应的复杂多样性。实验如下:
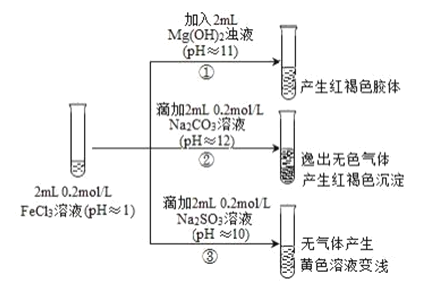
已知:含 Fe2+的溶液中加入 K3Fe(CN)6 溶液生成蓝色沉淀。K3Fe(CN)6 = 3K++Fe(CN)6 3-
(1)①中反应的离子方程式是______。
(2)写出②中发生反应的化学方程式______。
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加 BaCl2 溶液,产生白色沉淀。得出结论:FeCl3 与 Na2SO3 发生了氧化还原反应,其中SO32-被氧化生成了______(填离子的化学式)。
乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是取③中反应后的溶液,加入 K3Fe(CN)6 溶液,生成______(填蓝色沉淀的化学式,沉淀中不含钾元素),说明生成了 Fe2+。请写出 FeCl3 与 Na2SO3 溶液反应的离子方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示。
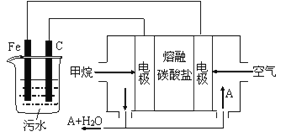
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的__________。
a.H2SO4 b.BaSO4 c.Na2SO4 d.NaOH
(2)电解池阳极发生了两个电极反应,电极反应式分别是
Ⅰ.___________________; Ⅱ._________________;
(3)电极反应Ⅰ和Ⅱ的生成物反应得到Fe(OH)3沉淀的离子方程式是__________________;
(4)该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。
①负极的电极反应是____________________;
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图)。A物质的化学式是_________________;
(5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)____L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com