
ЁОЬтФПЁПУОФмдкЖўбѕЛЏЬМжаШМЩеЃК2MgЃЋCO2![]() 2MgOЃЋCЃЌФЦБШУОИќЛюЦУЃЌФЧУДФЦФмдкЖўбѕЛЏЬМжаШМЩеТ№ЃПФГбаОПадбЇЯАаЁзщЩшМЦСЫШчЭМзАжУНјааЬНОПЁЃ
2MgOЃЋCЃЌФЦБШУОИќЛюЦУЃЌФЧУДФЦФмдкЖўбѕЛЏЬМжаШМЩеТ№ЃПФГбаОПадбЇЯАаЁзщЩшМЦСЫШчЭМзАжУНјааЬНОПЁЃ
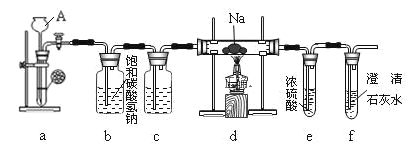
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉзАжУaжаЗЂЩњЕФЪЧЪЕбщЪвжЦCO2ЕФЗДгІЃЌЗДгІЗНГЬЪНЮЊ___ЁЃ
ЃЈ2ЃЉзАжУbжаЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ___ЃЌзАжУcЕФзїгУЮЊ___ЁЃ
ЃЈ3ЃЉЪЕбщЙ§ГЬжаЃЌдкЕуШМdзАжУжаЕФОЦОЋЕЦЧАЃЌБиаыОЙ§БивЊЕФВйзїЗНПЩНјааКѓајЕФЪЕбщЃЌИУБивЊЕФВйзїЪЧ___ЁЃ
ЃЈ4ЃЉЪЕбщЗЂЯжФЦдкГфТњЖўбѕЛЏЬМЦјЬхЕФВЃСЇЙмРяОчСвЕиШМЩеЃЌВњЩњДѓСПЕФАзбЬВЂАщгаКкЩЋЮяжЪЩњГЩЁЃШЁвЛВПЗжЩњГЩЮягкЪдЙмжаЃЌЭљЪдЙмжаМгЫЎЃЌАзЩЋЮяжЪШмНтгкЫЎЃЌКкЩЋЮяжЪВЛШмЁЃЙ§ТЫЃЌЕУЕНГЮЧхЕФТЫвКЁЃЭљЫљЕУТЫвКжаМгГЮЧхЪЏЛвЫЎЃЌШмвКБфЛызЧЁЃдйЕЮШыЯЁбЮЫсЃЌ ШмвКжагаЦјХнГіЯжЁЃЪдаДГіФЦгыЖўбѕЛЏЬМЗДгІЕФЛЏбЇЗНГЬЪНЃК___ЁЃ
ЁОД№АИЁП2HCl +CaCO3=CaCl2+H2O+CO2Ёќ H++HCO3-=H2O+CO2Ёќ ИЩдяCO2 ХХОЁгВжЪВЃСЇЙмжаЕФПеЦј 4Na+3CO2![]() 2Na2CO3 +C
2Na2CO3 +C
ЁОНтЮіЁП
ИљОнзАжУЃКAзАжУгЩЯЁбЮЫсгыЬМЫсбЮжЦБИЖўбѕЛЏЬМЦјЬхЃЌжЦЕУЕФЖўбѕЛЏЬМжаЛьгаHClКЭЫЎеєЦјЃЌBжаБЅКЭЬМЫсЧтФЦШмвКГ§ШЅHClЦјЬхЃЌcжаХЈСђЫсЮќЪеЫЎеєЦјЃЌИЩдяДПОЛЕФЖўбѕЛЏЬМгыNaдкdжаЗДгІЃЌдкЕуШМdзАжУжаЕФОЦОЋЕЦЧАЃЌБиаыГ§ШЅЯЕЭГФкЕФПеЦјЃЌЗРжЙФЦгыПеЦјжаЕФбѕЦјЗДгІЃЌfЗРжЙgжаЫЎеєЦјНјШыdзАжУЃЌgЗРжЙПеЦјжаЕФЖўбѕЛЏЬМНјШыdзАжУЃЌФЦгыЖўбѕЛЏЬМЗДгІЩњГЩСЫЬМЫсФЦКЭЬМЃЌОнДЫЗжЮізїД№ЁЃ
(1)ЪЕбщЪвгУЪЏЛвЪЏКЭЯЁбЮЫсЗДгІжЦШЁЖўбѕЛЏЬМЃЌЗДгІЗНГЬЪНЮЊЃК2HCl +CaCO3=CaCl2+H2O+CO2ЁќЃЌЙЪД№АИЮЊЃК2HCl +CaCO3=CaCl2+H2O+CO2ЁќЁЃ
(2)BжаБЅКЭЬМЫсЧтФЦШмвКГ§ШЅHClЦјЬхЃЌРызгЗНГЬЪНЮЊЃКH++HCO3-=H2O+CO2ЁќЃЛИљОнЗжЮіПЩжЊзАжУcЕФзїгУЪЧИЩдяЖўбѕЛЏЬМЃЌЙЪД№АИЮЊЃКH++HCO3-=H2O+CO2ЁќЃЛИЩдяCO2ЃЛ
(3)дкЕуШМdзАжУжаЕФОЦОЋЕЦЧАЃЌБиаыГ§ШЅЯЕЭГФкФкЕФПеЦјЃЌЗРжЙФЦгыПеЦјжаЕФбѕЦјЗДгІЃЌЙЪД№АИЮЊЃКХХОЁгВжЪВЃСЇЙмжаЕФПеЦјЃЛ
(4)ИУКкЩЋВЛШмЮяЮЊЬМЃЌЭЈЙ§ЖдЩњГЩЮяНјааСЫЬНОПЪЕбщПЩЕУГіФЦгыЖўбѕЛЏЬМЗДгІЩњГЩСЫЬМЫсФЦКЭЬМЃЌПЩвдаДГіЗДгІЕФЗНГЬЪНЃК4Na+3CO2 2Na2CO3 +CЃЌЙЪД№АИЮЊЃК4Na+3CO2
2Na2CO3 +CЃЌЙЪД№АИЮЊЃК4Na+3CO2 2Na2CO3 +CЁЃ
2Na2CO3 +CЁЃ


 УћХЦбЇаЃЗжВужмжмВтЯЕСаД№АИ
УћХЦбЇаЃЗжВужмжмВтЯЕСаД№АИ ЛЦИдКЃЕэШЋГЬХргХВтЪдОэЯЕСаД№АИ
ЛЦИдКЃЕэШЋГЬХргХВтЪдОэЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПСїЖЏЕчГиПЩвддкЕчГиЭтВПЕїНкЕчНтжЪШмвКЃЌДгЖјЮЌГжЕчГиФкВПЕчНтжЪШмвКХЈЖШЮШЖЈЃЌдРэШчЭМЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧ
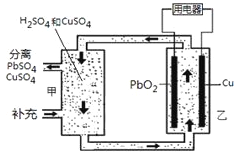
AЃЎCuЮЊИКМЋ
BЃЎPbO2ЕчМЋЕФЕчМЋЗДгІЪНЮЊЃКPbO2+ 4H++ SO42Ѓ+ 2eЃ= PbSO4+ 2H2O
CЃЎМзжагІВЙГфСђЫс
DЃЎЕБЯћКФ1 mol PbO2ЃЌашЗжРыГі2 mol CuSO4
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЭМЪЧСђЫсЪдМСЦПБъЧЉЩЯЕФВПЗжФкШнЁЃОнДЫЯТСаЫЕЗЈжае§ШЗЕФЪЧ(ЁЁЁЁ)
СђЫсЁЁЛЏбЇДПCP500 mL
ЦЗУћЃКСђЫс
ЛЏбЇЪНЃКH2SO4
ЯрЖдЗжзгжЪСПЃК98
УмЖШЃК1.84 gЁЄcmЃ3
жЪСПЗжЪ§ЃК98%
A.ИУСђЫсЕФЮяжЪЕФСПХЈЖШ18.0 molЁЄLЃ1
B.1molZnгызуСПЕФИУСђЫсЗДгІФмВњЩњ22.4L H2
C.ХфжЦ230mL4.6molЁЄLЃ1ЕФЯЁСђЫсашШЁИУСђЫс62.5mL
D.ШєВЛаЁаФНЋИУСђЫсНІЕНЦЄЗєЩЯЃЌгІСЂМДгУNaOHШмвКГхЯД
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЄгрЛдВФСЯдкЗЂЙтееУїЁЂНЛЭЈЕШСьгђОпгаЙуЗКЕФгІгУЧАОАЁЃЯТЭМЪЧвЛжжРћгУДѓРэЪЏ(жївЊГЩЗжCaCO3КЭMgCO3)КЭТСЭСПѓ(жївЊГЩЗжAl2O3ЃЌЛЙКЌЩйСПFe2O3дгжЪ)жЦБИвЛжжГЄгрЛдВФСЯ(Ca12Al14Ox)ЕФЙЄвеСїГЬЭМЁЃЛиД№ЯТСаЮЪЬтЃК

(1)Ca12Al14OxжаxЕФЪ§жЕЮЊ ______ЃЌЪдМСXЕФУћГЦЪЧ_________ЁЃ
(2)NH4ClШмвКФмШмНтЁАЗлФЉЁБЕФдвђЪЧ_________ЃЌЗЂЩњЕФжївЊЗДгІЕФЛЏбЇЗНГЬЮЊ______ЁЃ
(3)ЗДгІЂкЕФРызгЗНГЬЪНЮЊ _______ЁЃ
(4)ЪЕбщЪвМгШШAl(OH)3гІдк________(ЬювЧЦїУћГЦ)НјааЃЛВйзїЂйАќРЈ_____ЁЂИЩдяЕШЁЃ
(5)ШєШмвКМзжаc(Mg2+) <5ЁС10-5molL-1дЊЫиЫ№ЪЇЃЌДЫЪБгІЕїНкШмвКpHДѓгк______ЃЌЮЊМѕЩйИЦдЊЫиЫ№ЪЇЃЌгІПижЦШмвКМзжаc(Ca2+)Ём______ЁЃГЃЮТЯТKsp[Mg(OH)2]=5ЁС10Ѓ11ЃЌKsp[Ca(OH)2]=5ЁС10Ѓ6ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮяжЪЕФСПЪЧИпжаЛЏбЇжаГЃгУЕФЮяРэСПЃЌЧыЭъГЩвдЯТгаЙиЦфМЦЫуЕФФкШнЁЃ
ЃЈ1ЃЉ0.2 g H2КЌга___________________ИіHдзгЁЃ
ЃЈ2ЃЉ100 mL ФГAl2(SO4)3ШмвКжаЃЌc(Al3+) = 2.0 mol/LЃЌдђЦфжаc(SO42-) = _________mol/LЁЃ
ЃЈ3ЃЉЕШжЪСПЕФHClЁЂNH3ЁЂCO2ЁЂO2ЫФжжЦјЬхЃЌдкЯрЭЌЮТЖШКЭЯрЭЌбЙЧПЬѕМўЯТЃЌЬхЛ§зюДѓЕФЪЧ________ЁЃ
ЃЈ4ЃЉЕБCOЁЂCO2ЕФЗжзгИіЪ§жЎБШЮЊ1ЃК2ЪБЃЌдзгзмЪ§жЎБШЮЊ___________ЃЌжЪСПжЎБШЮЊ________ЃЛБъзМзДПіЯТЃЌУмЖШжЎБШЮЊ__________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГєбѕ(O3)жївЊЗжВМдкДѓЦјВуЕФЦНСїВужаЃЌФмЙЛЮќЪезЯЭтЯпЃЌБЛГЦЮЊЕиЧђЕФБЃЛЄЩЁЁЃЛиД№ЯТСаЮЪЬтЃК
(1)NOxЖдГєбѕВуЕФЦЦЛЕзїгУМЋДѓЃЌвбжЊЃКЂйNO+O3=NO2+O2 K1ЃЛNO2+O2=NO+O3ЃЛ K2ЃЛЂлO2+O=O3 K3ЃЌЗДгІ2O3=3O2ЕФЦНКтГЃЪ§K=_______ (гУK1ЁЂK2ЁЂK3БэЪО)ЃЌаДГівЛжжБЃЛЄГєбѕВуЕФДыЪЉ:__________ЁЃ
(2)гУГєбѕбѕЛЏбЬЦјжаЕФSO2ЕФжївЊЗДгІЮЊSO2(g)+O3(g)=SO3(g)+O2(g) ЁїHЃЌвбжЊЂй2SO2(g)+O2(g)=2SO3(g) ЁїH1=-198kJ/molЃЌЂк2O3(g)=3O2(g) ЁїH2=+284.2kJ/mol
ЂйЩЯЪіЗДгІжаЁїH= ____kJmol-1ЁЃ
ЂквЛЖЈЮТЖШЯТЃЌЯђ2LЙЬЖЈШнЛ§ЕФУмБеШнЦїжаМгШы2molO3КЭ2molSO2ЗЂЩњЩЯЪіЗДгІЃЌ5minКѓДяЕНЦНКтЃЌВтЕУШнЦїжаКЌга0.4molL-1SO3ЃЌДЫЪБSO2ЕФзЊЛЏТЪЮЊ_______ЃЌгћЬсИпO3ЕФРћгУТЪПЩВЩШЁЕФДыЪЉга_______(ЬюзжФИ)ЁЃ
a.ЪЪЕБдіДѓбЙЧП b.Щ§ИпЮТЖШ c.ЪЙгУгХжЪДпЛЏМС d.МАЪБЗжРыГіSO3
(3)ЙЄвЕЩЯгУCaSO3аќзЧвКЮќЪеЩЯЪізЊЛЏЩњГЩЕФSO3ПЩжЦБИЪЏИрЁЃвбжЊЃК298KЪБKsp(CaSO4)=9.0ЁС10Ѓ6ЃЌKsp(CaSO3)=1.5ЁС10Ѓ7ЃЌЯђ1LCaSO3аќзЧвКжаМгШыNa2SO4ЃЌШєга0.1molCaSO3ВЮгыЗДгІЃЌдђашМгШы_______molNa2SO4ЁЃ
 ЃЌ
ЃЌ
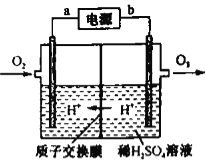
(4)ЙЄвЕЩЯПЩВЩгУЖшадЕчМЋЕчМЋЕчНтЯЁСђЫсЕФЗНЗЈжЦБИO3ЃЌЗДгІзАжУШчЩЯЭМЫљЪОЃЌЕчдДЕФaМЋЮЊ_____МЋЃЌЭЈШыO2ЕФЕчМЋЗДгІЪНЮЊ_______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПНЋ2.32gЬМЫсФЦЁЂЧтбѕЛЏФЦЕФЙЬЬхЛьКЯЮяЭъШЋШмНтгкЫЎЃЌжЦГЩШмвКЃЌШЛКѓЯђИУШмвКжаж№ЕЮМгШы1mol/LЕФбЮЫсЃЌЫљМгбЮЫсЕФЬхЛ§гыВњЩњCO2ЕФЬхЛ§(БъзМзДПі)ЙиЯЕШчЭМЫљЪОЃЌЯТСаЫЕЗЈжае§ШЗЕФЪЧ
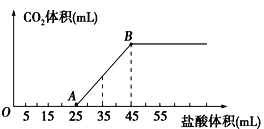
A.OAЖЮЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊЃКH++OH-=H2O
B.ЕБМгШы35mLбЮЫсЪБЃЌВњЩњCO2ЕФЬхЛ§ЮЊ224mL
C.AЕуШмвКжаЕФШмжЪЮЊNaC1ЁЂNa2CO3
D.ЛьКЯЮяжаNaOHЕФжЪСП0.60g
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПНЋ3mol/L NaOHШмвКЕЮШыЕН25mL вЛЖЈХЈЖШЕФAlCl3ШмвКжаЁЃЯТЭМЪЧећИіЙ§ГЬЕФЪ§бЇЗжЮіЧњЯпЁЃЦфжаКсжсБэЪОМгШыOH-ЕФЮяжЪЕФСПЃЌзнжсБэЪОВњЩњЕФAl(OH)3ГСЕэЕФЮяжЪЕФСПЁЃщЇЭМЛиД№ЃК
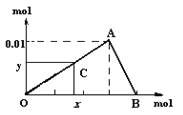
ЃЈ1ЃЉЕБCЕуДгOЕуЯђAЕудЫЖЏЪБЃЌБэЪОЫцOH-ЕФВЛЖЯМгШыЃЌГСЕэСПж№НЅ________ЁЃOAЧњЯпБэЪОЕФРызгЗДгІЪЧ________________ЃЌгЩДЫПЩЕУAЕуЕФзјБъЮЊ_______ЃЛ
ЃЈ2ЃЉЕБCЕуДгAЕуЯђBЕудЫЖЏЪБЃЌБэЪОЃК_____ЁЃABЧњЯпБэЪОЕФРызгЗДгІЮЊЃК______ЃЌгЩДЫПЩЕУBЕуЕФзјБъЮЊЃК__________ЁЃ
ЃЈ3ЃЉгЩЩЯЪіЗжЮіЃЌПЩЧѓЕУAlCl3ШмвКжаAl3+РызгЕФХЈЖШЮЊЃК_____mol/LЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПввЯЉЁЂЛЗбѕввдКЪЧживЊЕФЛЏЙЄдСЯЃЌгУЭОЙуЗКЁЃЛиД№ЯТСаЮЪЬтЃК
вбжЊЃКI.2CH2=CH2(g)+O2(g)![]() 2
2![]() (g) ЁїH1=-206.6kJmo1-1
(g) ЁїH1=-206.6kJmo1-1
II.CH2=CH2(g)+3O2(g)=2CO2(g)+2H2OЃЈ1ЃЉ ЁїH2
III.2![]() (g)+5O2(g)=4CO2(g)+4H2OЃЈ1ЃЉ ЁїH3
(g)+5O2(g)=4CO2(g)+4H2OЃЈ1ЃЉ ЁїH3
ЃЈ1ЃЉЗДгІIIIЃКЁїS(ЬюЁА>ЁБЁА<ЁБЛђЁА=ЁБ)___0ЁЃ
ЃЈ2ЃЉШШжЕЪЧБэЪОЕЅЮЛжЪСПЕФШМСЯЭъШЋШМЩеЪБЫљЗХГіЕФШШСПЃЌЪЧШМСЯжЪСПЕФвЛжжживЊжИБъЁЃвбжЊввЯЉЕФШШжЕЮЊ50.4kJg-1ЃЌдђЁїH3=___kJmol-1
ЃЈ3ЃЉЪЕбщВтЕУ2CH2=CH2(g)+O2(g)![]() 2
2![]() (g)жаЃЌvФц=kФцc2(
(g)жаЃЌvФц=kФцc2(![]() ЃЉЃЌvе§=kе§c2(CH2=CH2)c(O2)(kе§ЁЂkФцЮЊЫйТЪГЃЪ§ЃЌжЛгыЮТЖШгаЙиЃЉЁЃ
ЃЉЃЌvе§=kе§c2(CH2=CH2)c(O2)(kе§ЁЂkФцЮЊЫйТЪГЃЪ§ЃЌжЛгыЮТЖШгаЙиЃЉЁЃ
ЂйЗДгІДяЕНЦНКтКѓЃЌНіНЕЕЭЮТЖШЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ________ЃЉ
A.kе§ЁЂkФцОљдіДѓЃЌЧвkе§діДѓЕФБЖЪ§ИќЖр
B.kе§ЁЂkФцдШМѕаЁЃЌЧвkе§МѕаЁЕФБЖЪ§ИќЩй
C.kе§діДѓЁЂkФцМѕаЁЃЌЦНКте§ЯђвЦЖЏ
D.kе§ЁЂkФцОљМѕаЁЃЌЧвkФцМѕаЁЕФБЖЪ§ИќЩй
ЂкШєдк1LЕФУмБеШнЦїжаГфШы1molCH2=CH2(g)КЭ1molO2(g)ЃЌдквЛЖЈЮТЖШЯТжЛЗЂЩњЗДгІIЃЌОЙ§10minЗДгІДяЕНЦНКтЃЌЬхЯЕЕФбЙЧПБфЮЊдРДЕФ0.875БЖЃЌдђ0~10minФкv(O2)=___ЃЌ![]() =___ЁЃ
=___ЁЃ
ЃЈ4ЃЉЯжДњжЦБИввЯЉГЃгУввЭщбѕЛЏСбНтЗЈЃК
C2H6(g)+![]() O2(g)=C2H4(g)+H2O(g) ЁїH2=-110kJmol-1ЃЌЗДгІжаЛЙДцдкCH4ЁЂCOЁЂCO2ЕШИБВњЮяЃЈИБЗДгІОљЮЊЗХШШЗДгІЃЉЃЌЭМ1ЮЊЮТЖШЖдввЭщбѕЛЏСбНтЗДгІадФмЕФгАЯьЁЃ
O2(g)=C2H4(g)+H2O(g) ЁїH2=-110kJmol-1ЃЌЗДгІжаЛЙДцдкCH4ЁЂCOЁЂCO2ЕШИБВњЮяЃЈИБЗДгІОљЮЊЗХШШЗДгІЃЉЃЌЭМ1ЮЊЮТЖШЖдввЭщбѕЛЏСбНтЗДгІадФмЕФгАЯьЁЃ
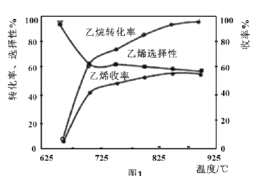
ЂйввЭщЕФзЊЛЏТЪЫцЮТЖШЕФЩ§ИпЖјЩ§ИпЕФдвђЪЧ___ЃЛЗДгІЕФзюМбЮТЖШЮЊ___ЃЈЬюађКХЃЉЁЃ
A.650Ёц B.700Ёц C.850Ёц D.900Ёц
ЃлввЯЉбЁдёад=![]() ЃЛввЯЉЪеТЪ=ввЭщзЊЛЏТЪЁСввЯЉбЁдёадЃн
ЃЛввЯЉЪеТЪ=ввЭщзЊЛЏТЪЁСввЯЉбЁдёадЃн
ЂкЙЄвЕЩЯЃЌБЃГжЬхЯЕзмбЙКуЖЈЮЊl00kPaЕФЬѕМўЯТНјааИУЗДгІЃЌЭЈГЃдкввЭщКЭбѕЦјЕФЛьКЯЦјЬхжаВєЛьЖшадЦјЬхЃЈЖшадЦјЬхЕФЬхЛ§ЗжЪ§ЮЊ70%)ЃЌВєЛьЖшадЦјЬхЕФФПЕФЪЧ___ЁЃ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com