
右下表为元素周期表的一部分,其中A、X、Y、W、Z为短周期元素,W元素的核电荷数为X元素的2倍。据此,下列说法中错误的是
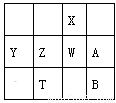
A. X、W、Z元素的原子半径与它们的气态氢化物的热稳定性变化趋势相反
B. Y、Z、W、A元素性质均较为活泼,但其中Y、W在自然界中存在游离态的形式,它们的最高价氧化物的水化物的酸性依次递增
C. 工业上电解A的钠盐溶液可以得到多种产物,为防止产物互相反应常使用阳离子交换膜,其阴极反应式为:2H2O+2e-=2OH-+H2↑
D. 根据元素周期律,可以推测T元素的单质具有半导体特性,T2W3具有氧化性和还原性
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案科目:高中化学 来源:2016届福建省高三下模拟考试理综化学试卷(解析版) 题型:推断题
绿原酸是金银花的主要抗菌、抗病毒有效药理成分之一。
Ⅰ.已知绿原酸X的结构简式为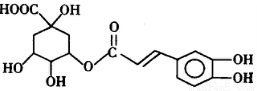
(1)X中含氧原子的官能团的名称为____ _。
(2)下列叙述正确的是 _。
①X的分子式为C16O20O9
②1molX最多能与4mol H2发生加成反应
③X能与碳酸氢钠溶液反应,且能使酸性高锰酸钾褪色
④1molX最多能与5mol NaOH反应
⑤绿原酸水解后所得两产物碳原子数之差为2
Ⅱ.绿原酸在一定条件下可合成D和对羟基苯甲酸两种医药中间体,其合成路线如下(部分反应条件未注明):
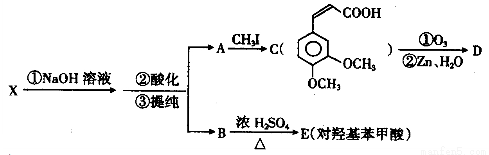
已知:R—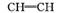 —R
—R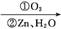 2R—CHO
2R—CHO
(1) D是一种芳香族化合物,D的结构简式为 ;
(2)A→C的反应类型是 ;
(3)由B生成E的化学方程式为 ;
(4)F与E互为同分异构体,且F同时满足下列条件:
①遇氯化铁溶液显紫色
②能发生银镜反应
③核磁共振氢谱为4组峰,且面积比为2:2:1:1,则F的结构共有 种(不考虑立体异构),结构简式为 (任写一种)
查看答案和解析>>
科目:高中化学 来源:2016届吉林省长春十一高三下考前冲刺理综化学试卷二(解析版) 题型:选择题
Wolff-Kishner-黄鸣龙反应是醛类或酮类在碱性条件下与肼作用,使得>C=O转化为-CH2-。如:
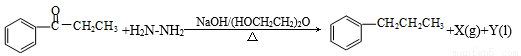
其中,X和Y不污染环境,下列说法中不正确的是( )
A.肼作还原剂
B.X是N2
C.Y是H2O
D.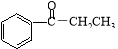 在酸性条件下水解为苯甲酸和乙醇
在酸性条件下水解为苯甲酸和乙醇
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:实验题
苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱之一。下面是它的一种实验室合成路线:
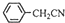 +H2O+H2SO4
+H2O+H2SO4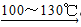
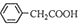 +NH4HSO4
+NH4HSO4
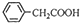 +Cu(OH)2→(
+Cu(OH)2→(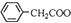 )2Cu+H2O
)2Cu+H2O
已知:苯乙腈的熔点为-23℃,不溶于水;
苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇.
回答下列问题:
(1)制备苯乙酸的装置示意图如图(加热和夹持装置等略):在250mL三口瓶a中加入70mL 70%硫酸.配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是__________;
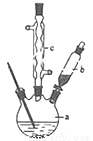
(2)将a中的溶液加热至100℃,再由b缓缓滴加40g苯乙腈到硫酸溶液中,然后升温至130℃继续反应.在装置中,仪器c的名称是__________;其作用是__________;
(3)反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是__________,下列仪器中可用于分离苯乙酸粗品的是__________;
A.分液漏斗 |
B.漏斗 |
C.烧杯 |
D.直形冷凝管 |
E.玻璃棒
(4)提纯苯乙酸的方法是__________,最终得到44g纯品,则苯乙酸的产率是__________;
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是__________;
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:选择题
常温下,饱和NaClO溶液的pH约为11。某消毒液的主要成分为NaClO,洁厕灵主要成分为HCl。下列解释相关事实的离子方程式中不合理的是
A.该消毒液加白醋生成HClO,可增强消毒能力:H++ClO-=HClO
B.该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-=ClO-+Cl-+H2O
C.常温下,该消毒液的pH≈11,是因为:ClO-+H2O HClO+OH-
HClO+OH-
D.该消毒液与洁厕灵混用会引起中毒:2H++Cl-+ClO-=Cl2↑+H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二5月月考化学试卷(解析版) 题型:选择题
设NA表示阿伏加罗常数的值,下列说法正确的是
A.常温下,1L0.1mol•L-1CuSO4溶液中含有的Cu2+数目为0.1NA
B.含1molCl-的NH4Cl溶液中加入适量氨水使溶液呈中性,此时溶液NH4+为NA
C.2mol SO2与足量氧气在适当的条件下反应生成SO3,转移的电子数为4NA
D.25°C时,1L pH=1的硫酸溶液中,含有H+的数目为0.2NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省宁波市高一下期中化学试卷(解析版) 题型:选择题
参照反应Br+H2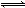 HBr+H的能量对应反应过程的示意图,下列叙述中正确的是( )
HBr+H的能量对应反应过程的示意图,下列叙述中正确的是( )
A.正反应为吸热反应
B.吸热反应一定要加热后才能发生
C.反应物总能量高于生成物总能量
D.升高温度可增大正反应速率,降低逆反应速率
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一下第二次月考化学试卷(解析版) 题型:选择题
据报道,我国拥有完全自主产权的氢氧燃料电池车已在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液。下列有关该电池的叙述不正确的是( )
A.正极反应式为:O2+2H2O+4e-===4OH-
B.工作一段时间后,电解液中KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2===2H2O
D.该电池工作时每消耗1 mol O2,有2 mol电子转移
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com