
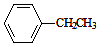
 $→_{加热}^{Fe_{2}O_{3}}$
$→_{加热}^{Fe_{2}O_{3}}$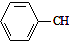 =CH2+H2,下列说法正确的是( )
=CH2+H2,下列说法正确的是( )| A. | 酸性高锰酸钾溶液和溴水都可以用来鉴别乙苯和苯乙烯 | |
| B. | 乙苯、苯乙烯均能发生取代反应、加聚反应,氧化反应 | |
| C. | 乙苯的一氯取代产物有共有5种 | |
| D. | 乙苯和苯乙烯分子内共平面的碳原子数最多均为7 |
分析 由乙苯生产苯乙烯,H原子减少,为消去反应,苯环、碳碳双键为平面结构,苯乙烯中含碳碳双键具有烯烃的性质,以此来解答.
解答 解:A.乙苯和苯乙烯均能被高锰酸钾氧化,现象相同,不能鉴别,故A错误;
B.乙苯不含碳碳双键,不能发生加聚反应,故B错误;
C.苯环有3种H,乙基有2种H,则乙苯的一氯取代产物有共有5种,故C正确;
D.苯环和碳碳双键都为平面结构,与苯环直接相连的原子在同一个平面上,则乙苯有7个碳原子共平面,考虑三点确定一个平面,则可能有八个碳共平面,苯乙烯有8个碳原子共平面,故D错误.
故选C.
点评 本题考查有机物结构和性质,为高频考点,侧重于学生的分析能力的考查,明确官能团与性质关系即可解答,侧重考查基本概念、烯烃、基本反应类型等知识点,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11g CO2含有的共用电子对数为0.5NA | |
| B. | 1mol Na分别与足量的O2反应生成Na2O或Na2O2,失去的电子数均为NA | |
| C. | 通常状况下,39 g Na2O2固体中含有的离子总数为2NA | |
| D. | 滴加到沸水中的FeCl3溶液有5.6 g Fe3+发生水解,则生成的胶粒数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 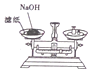 称取一定量的NaOH | |
| B. | 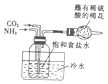 制取NaHCO3 | |
| C. | 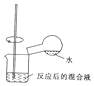 检验浓硫酸与铜反应后的产物中是否含有铜离子 | |
| D. | 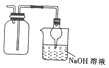 收集NO2丙防止其污染环境 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下90g乙二酸所占的体积约为22.4L | |
| B. | lmol乙二酸中含有共用电子对的数目为9NA | |
| C. | 90g乙二酸被NaC1O氧化生成CO2,转移的电子数为NA | |
| D. | 0.lmol•L-1的乙二酸溶液中,H2C2O4、C2O2-和HC2O4-的微粒数之和为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-═CO2↑+H2O | |
| B. | 铁和稀硫酸反应:Fe+2H+═H2↑+Fe3+ | |
| C. | 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-═CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
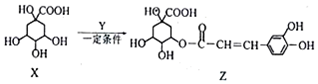
| A. | X能使酸性高锰酸钾溶液褪色 | |
| B. | Y的分子式为C9H8O3 | |
| C. | 1mol Z与足量NaOH溶液反应,最多消耗8mol NaOH | |
| D. | Z与浓溴水既能发生取代反应又能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  如图装置可用于制备氢氧化亚铁 | |
| B. | 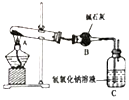 如图装置可用于测定Na2CO3和NaHCO3混合物中NaHCO3的含量 | |
| C. |  如图装置可用于检验氨气溶于水后显碱性 | |
| D. |  如图装置可用于CaCO3和稀盐酸反应制取少量的CO2气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com