
| A、化学键断裂时要吸收能量,形成新化学键时要放出能量 |
| B、化学变化的实质是旧化学键断裂,新化学键形成 |
| C、在化学变化过程中,一定要吸收或放出能量 |
| D、吸收能量或放出能量的过程,一定是化学变化过程 |


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属氧化物都能与水反应生成碱 |
| B、非金属氧化物都能与水反应生成酸 |
| C、氧化铝既能与酸反应又能与氨水反应 |
| D、氧化铝坩埚不能用于熔融烧碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
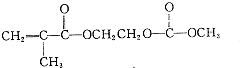
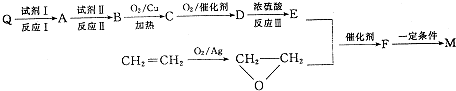
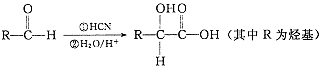
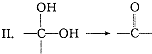
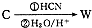 ,请写出符合下列条件的w的一种同分异构体的结构简式
,请写出符合下列条件的w的一种同分异构体的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A 基态原子有3个能级,各能级中电子数相等 |
| B 基态原子核外有13种不同运动状态的电子 |
| C与B处于同一周期,且原子在该周期中电负性最大 |
| D D4+的核外电子排布与氩原子相同 |
| E 是ds区原子序数最小的元素 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com