
| A、金属钠和水:2Na+2 H2O=2Na++2OH-+H2↑ |
| B、铜和浓硝酸:Cu+4 H++2NO3-=Cu2++2NO2↑+2 H2O |
| C、Cl2通入水中:Cl2+H2O=H++Cl-+HClO |
| D、硫酸铜溶液和氢氧化钡溶液:SO42-+Ba2+=BaSO4↓ |


科目:高中化学 来源: 题型:
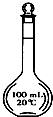 把18.0mol/L 的浓硫酸稀释成1.80mol/L 的稀硫酸100mL,实验操作如下:
把18.0mol/L 的浓硫酸稀释成1.80mol/L 的稀硫酸100mL,实验操作如下:查看答案和解析>>
科目:高中化学 来源: 题型:
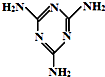 食品安全关系国计民生,影响食品安全的因素很多.
食品安全关系国计民生,影响食品安全的因素很多.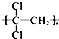 ,具有超强的阻隔性能,可作为保鲜食品的包装材料,它是由
,具有超强的阻隔性能,可作为保鲜食品的包装材料,它是由查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | Z | W | R |
| +4-4 | -2 | +1 | +3 | +7-1 |
| A、原子半径:Z>X>Y |
| B、R的含氧酸的酸性一定强于X的含氧酸的酸性 |
| C、X和Y可形成多种共价化合物 |
| D、工业上用电解W的氧化物的方法制备单质W |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6g时,放出19.12kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6kJ.mol-1 |
| B、稀醋酸与0.1mol?L-1NaOH溶液反应:H+(aq)+OH-(aq)═H2O(l)△H=57.3kJ?mol-1 |
| C、已知1mol氢气完全燃烧生成液态水所放出的热量为285.5kJ,则水分解的热化学方程式:2H2O(l)═2H2(g)+O2(g)△H=+285.5kJ.mol-1 |
| D、已知2C(s)+O2(g)═2CO(g)△H=-22.1kJ.mol-1则可知C的燃烧热△H=-110.5kJ.mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
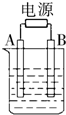 如图用石墨作电极的电解池中,放入某足量蓝色溶液500mL进行电解,观察到A电极表面有红色固体生成,B电极有无色气体生成;通电一段时间后,取出A电极,洗涤、干燥、称量,A电极增重1.6g.下列说法错误的是( )
如图用石墨作电极的电解池中,放入某足量蓝色溶液500mL进行电解,观察到A电极表面有红色固体生成,B电极有无色气体生成;通电一段时间后,取出A电极,洗涤、干燥、称量,A电极增重1.6g.下列说法错误的是( )| A、图中B极同电源正极相连 |
| B、该蓝色溶液可能是Cu(NO3)2或CuCl2溶液 |
| C、电解后溶液的pH约为1(溶液体积变化忽略不计) |
| D、要使电解后溶液恢复到电解前的状态,则可加入2gCuO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升高温度只提高逆反应速率 |
| B、降低温度可提高正反应速率 |
| C、使用催化剂能显著增大反应速率 |
| D、达到化学平衡时正、逆反应速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com