
下列说法不正确的是 )。
①非金属元素构成的单质中一定存在共价键;②非金属之间形成的化合物一定是共价化合物;③非金属的气态氢化物中一定存在极性共价键;④离子化合物中一定含有离子键;⑤金属元素和非金属元素形成的化合物一定是离子化合物;⑥在一种化合物中只能存在一种类型的化学键;⑦含共价键的化合物不一定是共价化合物;⑧含离子键的化合物一定是离子化合物;⑨氯化钠和HCl溶于水都发生电离,克服粒子间作用力的类型相同
A.③④⑦⑧ B.①③④⑦⑧
C.①②⑤⑥⑨ D.①④⑦⑨
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.在一定温度下AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数
B.AgCl的Ksp=1.8×10-10 mol2·L-2,在任何含AgCl固体的溶液中,[Ag+]=[Cl-]且Ag+与Cl-浓度的乘积等于1.8×10-10 mol2·L-2
C.温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液
D.向饱和AgCl水溶液中加入盐酸,Ksp值变大
查看答案和解析>>
科目:高中化学 来源: 题型:
把0.02 mol·L-1 CH3COOH溶液和0.01 mol·L-1 NaOH溶液以等体积混合,溶液呈酸性,混合溶液中粒子浓度关系正确的是( )
A.[CH3COO-]>[Na+]
B.[CH3COOH]>[CH3COO-]
C.2[H+]=[CH3COO-]-[CH3COOH]
D.[CH3COOH]+[CH3COO-]=0.02 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,向20 mL 0.1 mol·L-1CH3COOH溶液中逐滴加入0.1 mol·L-1NaOH溶液,其pH变化曲线如图所示忽略温度变化)。下列说法中错误的是 )。
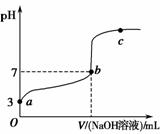
A.a与b之间的溶液中只存在:cCH3COO-)>cNa+)>cH+)>cOH-)
B.b与c之间的溶液中不存在:cCH3COO-)>cH+)>cNa+)>cOH-)
C.b点时,VNaOH溶液)<20 mL,且cCH3COO-)=cNa+)
D.a、b、c点表示的溶液中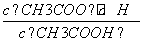 均相等
均相等
查看答案和解析>>
科目:高中化学 来源: 题型:
20 mL 0.1 mol·L-1溶液中含有Fe2+,向其中滴加NaOH溶液至pH=4,溶液中有沉淀生成,过滤,得沉淀和滤液。已知:Ksp[FeOH)3]=4.0×10-38,Ksp[FeOH)2]=8.0×10-16。下列说法不正确的是 )。
A.沉淀只有FeOH)3
B.沉淀有FeOH)3和FeOH)2
C.滤液cFe3+)=4.0×10-8 mol·L-1
D.向滤液中滴加FeCl2溶液,无沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s)NH3(g)+HI(g);
②2HI(g)H2(g)+I2(g)
达到平衡时,c(H2)=0.5 mol·L-1,c(HI)=4 mol·L-1,则此温度下反应①的平衡常数为( )
A.9 B.16
C.20 D.25
查看答案和解析>>
科目:高中化学 来源: 题型:
2NO(g) +O2(g)2NO2(g) 。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
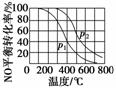
①比较p1、p2的大小关系________。
②随温度升高,该反应平衡常数变化的趋势是________。
(2)[2014·广东理综,31(2)(3)(4)]用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
① 1/4CaSO4(s)+CO(g)1/4CaS(s)+CO2(g) ΔH1=-47.3 kJ·mol-1
② CaSO4(s)+CO(g)CaO(s)+CO2(g) +SO2(g) ΔH2=+210.5 kJ·mol-1
③ CO(g)1/2C(s)+1/2CO2(g) ΔH3=-86.2 kJ·mol-1
①反应①~③的平衡常数的对数lgK随反应温度T的变化曲线见下图,结合各反应的ΔH,归纳lgK~T曲线变化规律:

a.__________________________________________________________;
b.__________________________________________________________。
②向盛有CaSO4的真空恒容密闭容器中充入CO,反应①于900 ℃达到平衡,c平衡(CO)=8.0×10-5 mol·L-1,计算CO的转化率(忽略副反应,结果保留两位有效数字)。
③为减少副产物,获得更纯净的CO2,可在初始燃料中适量加入________。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:

(1)气体A中的大气污染物可选用下列试剂中的_________吸收。
a.浓硫酸 b.稀硝酸
c.NaOH溶液 d.氨水
(2)用稀硫酸浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在_______(填离子符号),检验溶液中还存在Fe2+的方法是____________(注明试剂、现象)。
(3)由泡铜冶炼粗铜的化学方程式为_________________________________。
(4)以CuSO4溶液 为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的
为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的 是__________。
是__________。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(5)利用反应2Cu+O2+2H2SO4====2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.向蔗糖水解后的溶液中直接加入少量银氨溶液,可证明生成了葡萄糖
B.淀粉与纤维素、葡萄糖与果糖均互为同分异构体
C.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
D.在浓硫酸存在下,苯与浓硝酸共热生成硝基苯的反应属于取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com