
选考【化学—选修5:有机化学基础】 (15分)
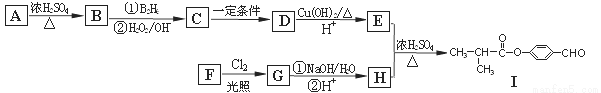
有机物Ⅰ可以用E和H在一定条件下合成:
请根据以下信息完成下列问题:
①A为丁醇且核磁共振氢谱有2种不同化学环境的氢;
②
③一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
(1)B的分子式为: 。
(2)C→D、G→H的反应类型为 、 。
(3)芳香族化合物F的分子式为C7H8O,苯环上的一氯代物只有两种,则F的结构简式为: 。
(4)D生成E的化学方程式为 。
E与H反应生成I的方程式为 。
(5)I的同系物K相对分子质量比I小28。K的结构中能同时满足如下条件:①苯环上只有两个取代基;②分子中不含甲基。共有 种(不考虑立体异构)。试写出上述同分异构体中任意一种消耗NaOH最多的有机物结构简式 。
(15分)
(1)C4H8(1分)
(2)氧化反应(1分)、水解反应(1分)
(3) (2分)
(2分)
 (4)
(4) (3分)
(3分)
 (3分)
(3分)
(5)12种(2分);  (2分)(邻、间、对任写一种即可)
(2分)(邻、间、对任写一种即可)
【解析】
试题分析:因为A为丁醇且核磁共振氢谱有2种不同化学环境的氢,则A为2-甲基-2-丙醇,结构简式为:(CH3)3C-OH,A在浓硫酸条件下加热发生消去反应,生成的B为2-甲基丙烯,根据信息②B转化为C:2-甲基-1-丙醇,D能与Cu(OH)2反应,则D为2-甲基丙醛,E为2-甲基丙酸,根据I的结构可推出H为HO— —CHO,根据芳香族化合物F的分子式为C7H8O, 苯环上的一氯代物只有两种,可知F为:
—CHO,根据芳香族化合物F的分子式为C7H8O, 苯环上的一氯代物只有两种,可知F为: ,G为HO—
,G为HO— —CHCl2。
—CHCl2。
(1)B为2-甲基丙烯,分子式为C4H8。
(2)C→D为2-甲基-1-丙醇转化为2-甲基丙醛,反应类型为氧化反应;G→H为HO— —CHCl2转化为HO—
—CHCl2转化为HO— —CHO,反应类型为水解反应。
—CHO,反应类型为水解反应。
(3)根据上述分析,F的结构简式为: 。
。
(4)D生成E,为2-甲基丙醛与新制氢氧化铜反应生成2-甲基丙酸,所以化学方程式为:
 ;
;
E与H反应生成I,E中的羧基与H中的羟基发生酯化反应,所以化学方程式为:
 。
。
(5)I的同系物K相对分子质量比I小28,则K比I少2个CH2原子团,根据①苯环上只有两个取代基;②分子中不含甲基可知,两个取代基可能为HCOO—和—CH2CHO,或HCOO CH2—和—CHO,或HOOC—和—CH2CHO,或HOOCCH2—和—CHO,四种情况,两个取代基邻、间、对各3种,所以K的结构共12种;消耗NaOH最多的有机物的结构是取代基为HCOO—和—CH2CHO,因为HCOO—水解可得羧基和酚羟基,都能消耗NaOH,两种取代基邻、间、对任写一种即可。
考点:本题考查有机合成的分析与推断、反应类型的判断、同分异构体。


科目:高中化学 来源:2014-2015安徽省淮南市高二上学期期末考试化学(理)试卷(解析版) 题型:选择题
锅炉水垢是一种安全隐患,除去水垢中的CaSO4,可先用Na2CO3溶液处理,使之转化为易溶于酸的CaCO3,再用酸除去。下列说法不正确的是
A.CaCO3的溶解度小于CaSO4
B.沉淀转化的实质是沉淀溶解平衡的移动
C.沉淀转化的难易与溶解度差别的大小无关
D.CaSO4到CaCO3的沉淀转化中并存着两个沉淀溶解平衡
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省濮阳市高二上学期第三次月考化学试卷(解析版) 题型:选择题
对于密闭容器中进行的反应CO(g) + H2O(g) CO2 (g) +H2 (g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是
CO2 (g) +H2 (g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是
A.正反应速率增大
B.逆反应速率减小
C.达到平衡时,逆反应速率比原平衡要大
D.化学平衡常数不变
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省濮阳市高二上学期第三次月考化学试卷(解析版) 题型:选择题
0.1mol/L的K2S溶液中,有关粒子的浓度大小关系正确的是
A.c(K+)+c(H+)=c(S2—)+c(HS—)+c(OH—) B.c(H+)= c(OH—)
C.c(K+)=c(S2—)+c(HS—)+c(H2S) D.c(OH-)=c(H+)+c(HS—)+2c(H2S)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省弥勒市高三市统测一模理综化学试卷(解析版) 题型:填空题
(14分)
(1)已知:① N2(g) + O2(g)=2NO(g) △H=+179.5 kJ/mol
②2NO(g) + O2(g)=2NO2(g) △H=-112.3 kJ/mol
③2NO(g) +2CO(g)=N2(g) +2CO2(g) △H=-759.8 kJ/mol
NO2(g)+CO(g)=NO(g) +CO2(g) △H= kJ/mol。
(2)将不同物质的量的H2O(g)和CO(g)分别通入体积为2L的恒容密闭容器中,
进行反应:H2O(g)+CO(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | CO | H2 | |||
① | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
② | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
③ | 900 | a | b | c | d | t |
①实验组①中以v(CO2)表示的反应速率为 ,此温度下的平衡常数为 ,温度升高时平衡常数会 (填“增大”、“减小”或“不变”)。
②650℃时,若在此容器中开始充入2mol H2O(g)、1mol CO、1 mol CO2和 2 molH2,若要使反应在开始
时 进行。(填“正向”、“逆向”)
③若a=2,b=1,则c= ,达平衡时实验组②中H2O(g)和实验组③中CO的转化率的关系
为α2 (H2O) α3 (CO)(填“<”、“>”或“=”)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省弥勒市高三市统测一模理综化学试卷(解析版) 题型:选择题
化学在生产和日常生活中有着重要的应用。下列叙述正确的是
A.在有机化工中,氯气是合成塑料、橡胶、农药和人造纤维的重要原料
B.汽车尾气中含有氮的氧化物,是汽油不完全燃烧造成的
C.白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去
D.油脂是产生能量很高的营养物质,在饮食中不必控制油脂的摄入量
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省景德镇市高三第二次质检理综化学试卷(解析版) 题型:填空题
(12分)
Ⅰ、按要求写出下列反应的方程式:
(1)碳酸氢铵与少量的氢氧化钠溶液反应(离子方程式) 。
(2)氯化铁溶液中通入二氧化硫气体(离子方程式) 。
(3)一定量的硫酸铝钾加入氢氧化钡溶液生成沉淀质量最大时的反应(化学方程式) 。
(4)碘化亚铁和氯气以5:7的物质的量比反应(化学方程式) 。
Ⅱ、已知Fe2O3在高炉中有下列反应:Fe2O3+CO=2FeO+CO2,反应形成的固体混合物(Fe2O3和FeO)中,元素铁和氧的质量比用m(Fe):m(O)表示。
(1)上述固体混合物中,m(Fe):m(O)可能是 。
a.7:5 b.3:1 c.7:1
(2)设Fe2O3被CO还原的百分率为A%,则用含m(Fe)、m(O)的代数式表示A%的关系式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省苏州市高三上学期期末调研测试化学试卷(解析版) 题型:选择题
下图为“长式元素周期表”的一部分,其中短周期元素W、X、Y、Z的位置关系如图。下列说法一定正确的是
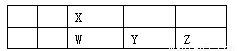
A.元素Z位于元素周期表的第3周期ⅦA族
B.原子半径的大小顺序为:rY>rW>rX
C.元素W的最高价氧化物对应水化物的酸性比Y的强
D.元素X的气态简单氢化物的热稳定性比W的强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com