
��֪�Ȼ�ѧ����ʽ(Q1��Q2��Ϊ��ֵ)��C(s)��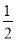 O2(g)=CO(g)����H����Q1kJ��mol��1��C(s)��O2(g)=CO2(g)����H����Q2 kJ��mol��1���й�������Ӧ������������ǣ� ��
O2(g)=CO(g)����H����Q1kJ��mol��1��C(s)��O2(g)=CO2(g)����H����Q2 kJ��mol��1���й�������Ӧ������������ǣ� ��
A��Q1��Q2
B�������������������ڷ�Ӧ��������
C����1 mol C��Ӧ����1 mol CO����ʱ�ų�Q1 kJ����
D��1 mol CO2������е���������1 mol�ɱ����е�����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��8-2��ϰ���������棩 ���ͣ�ѡ����
���ڳ�����pHΪ1��������Һ������������ȷ���ǣ� ��
A������Һ1 mLϡ����100 mL��pH����3
B�������Һ�м���pHΪ13������������Һǡ����ȫ�к�
C������Һ������������c(H��)��ˮ�������c(H��)֮��ֵΪ10��12
D������Һ��ˮ�������c(H��)��pHΪ3��������ˮ�������c(H��)��100��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��7-2��ϰ���������棩 ���ͣ�ѡ����
��100 ��ʱ����0.40 mol���������������2 L�ܱ������У�ÿ��һ��ʱ��Ը�������
�����ʽ��з������õ��������ݣ�
ʱ��(s) | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
����˵������ȷ���ǣ� ��
A����Ӧ��ʼ20 s���Զ���������ʾ��ƽ����Ӧ����Ϊ0.001 25 mol��L��1��s��1
B��80 sʱ����������ɫ��60 sʱ��ͬ����40 sʱ����ɫ��
C��80 sʱ�������м���0.32 mol������ͬʱ����������Ϊ4 L����ƽ�⽫���ƶ�
D������ʼͶ��Ϊ0.20 mol N2O4����ͬ�����´�ƽ�⣬�����ֺ�����ԭƽ����ϵ��Ӧ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��7-1��ϰ���������棩 ���ͣ�ѡ����
�����йػ�ѧ��Ӧ���ʵ�˵������ȷ���ǣ� ��
A����ѧ��Ӧ�ﵽ�����ʱ�����淴Ӧ����Ҳ�ﵽ��������
B�������ܽ��ͻ�ѧ��Ӧ�Ļ�ܣ��ӿ췴Ӧ���ʣ��������Ч��
C����п��ϡ���ᷴӦ��ȡH2ʱ���μӼ�������ͭ��Һ�ܼӿ췴Ӧ����
D������Ƭ��ϡ���ᷴӦ��H2����98%��Ũ�������H2�����ʿ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��6-1��ϰ���������棩 ���ͣ�ѡ����
��֪����1 mol H2��1 mol Cl2�еĻ�ѧ�����յ������ֱ�Ϊ436 kJ��243 kJ������H
ԭ�Ӻ�Clԭ���γ�1 mol HClʱ�ͷŵ�����Ϊ431 kJ���������Ȼ�ѧ����ʽ����ȷ���ǣ� ��
A��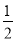 H2(g)��
H2(g)��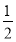 Cl2(g)=HCl(g) ��H����183 kJ��mol��1
Cl2(g)=HCl(g) ��H����183 kJ��mol��1
B��H2(g)��Cl2(g)=2HCl(g)����H����183 kJ��mol��1
C��HCl(g)= 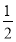 H2(g)��
H2(g)��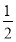 Cl2(g) ��H����91.5 kJ��mol��1
Cl2(g) ��H����91.5 kJ��mol��1
D��H2(g)��Cl2(g)=2HCl(g)����H����248 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��5-3��ϰ���������棩 ���ͣ������
��֪X��Y�������ӣ�Z�������ӣ�M��N�Ƿ��ӣ����Ƕ��ɶ�����Ԫ����ɣ��Ҿ���
���½ṹ���������ʣ�
��X��Y��M��N�ĺ������������ȣ��������£�M�Ǽ�������N�����壻��X��M������ͬ��Ԫ����ɣ���YΪ�������ӣ�����Z��ɵ����ʿ����ھ�ˮ����Z��ͬ����Ԫ����ɡ���ش��������⣺
(1)X�ĵ���ʽΪ ��Z�����ӷ���Ϊ ��
(2)X��Z�γɵĻ������������еĻ�ѧ������Ϊ ��
(3)д��Y��M��N�γɵĻ�������Ӧ�����ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��5-3��ϰ���������棩 ���ͣ�ѡ����
�ס��ҡ��������������ʾ�Ϊֻ������Ԫ�صĻ�����Ҿ���18�����ӡ������й���
�������ʵ��ƶϣ���ȷ���ǣ� ��
A��������ij�������к������Ӽ�
B���������ʶ��ǹ��ۻ�����
C���������ʶ������ܾ���ǿ������
D����һ�������������ͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��5-2��ϰ���������棩 ���ͣ�ѡ����
����ʵ�鲻�ܴﵽԤ��Ŀ�ĵ��ǣ� ��
���ʵ�����ʵ��Ŀ��
ACl2��Br2�ֱ���H2��Ӧ�Ƚ��ȡ���ķǽ�����ǿ��
BMgCl2��AlCl3��Һ�зֱ�ͨ��NH3�Ƚ�þ�����Ľ�����ǿ��
C�ⶨͬŨ�ȵ�Na2CO3��Na2SO4��Һ��pH�Ƚ�̼����ķǽ�����ǿ��
DFe��Cu�ֱ������ᷴӦ�Ƚ�����ͭ�Ľ�����ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧһ�ָ�ϰ�κ�淶ѵ��4-3��ϰ���������棩 ���ͣ�ѡ����
����������ʹƷ����Һ��ɫ������ɫԭ��������ͬ���ǣ� ��
������̿������ˮ������������������������������������˫��ˮ
A���٢ڢ� B���ڢۢ� C���ڢܢݢ� D���٢ڢۢܢݢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com