
| A. | 夏天打开啤酒瓶,有大量气泡逸出 | |
| B. | 对于反应I2(g)+H2(g)?2HI(g)达到平衡后,增大压强气体颜色加深 | |
| C. | 紫色CoCl2溶液,加热溶液颜色变为蓝色,用冰水冷却溶液颜色变为粉红色 | |
| D. | 工业合成氨(N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol)选择高压条件 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动.使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答 解:A.因溶液中存在二氧化碳的溶解平衡,打开汽水瓶后,压强减小,二氧化碳逸出,能用勒夏特列原理解释,故A不选;
B.该反应的反应前后气体计量数之和不变,增大压强容器体积减小,碘浓度增大,气体颜色加深,但增大压强平衡不移动,不能用平衡移动原理解释,故B选;
C.存在平衡Co(H2O)62+[粉红色]+4Cl-?6H2O+CoCl42-[蓝色]△H>0,升高温度平衡正向移动,溶液颜色变为蓝色,降低温度平衡逆向移动,溶液颜色变为粉红色,所以可以用平衡移动原理解释,故C不选;
D.该反应是一个反应前后气体体积减小的可逆反应,增大压强平衡正向移动,可以用平衡移动原理解释,故D不选;
故选B.
点评 本题考查化学平衡移动原理,为高频考点,明确平衡移动原理内涵是解本题关键,注意平衡移动原理适用范围,题目难度不大,易错选项是B.


科目:高中化学 来源: 题型:选择题
| A. | C6H13OH和C5H11OH | B. | C6H13OH | ||
| C. | C5H11OH | D. | C11H23OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.8 g | B. | 4.8 g | C. | 5.4 g | D. | 6.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 Q2=Q1 | B. | 2 Q2>Q1 | C. | 2 Q2<Q1<Q | D. | Q=Q1>Q2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol Cl2所占体积约为11.2 L | |
| B. | 16 g O2中含有的分子数约为6.02×1023 | |
| C. | 0.1 mol/L NaCl溶液中含溶质的物质的量为0.1 mol | |
| D. | 标准状况下,11.2 L N2和CO的混合气体所含原子数约为6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 500 mL溶液中Ba2+和Cl-总数为0.3NA | |
| B. | 500 mL溶液中Ba2+浓度为0.2 mol•L-1 | |
| C. | 500 mL溶液中Cl-总数为0.2 NA | |
| D. | 500 mL溶液中Cl-浓度为0.2 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将40g NaOH溶于1L水中,所得NaOH溶液的浓度为1mol•L-1 | |
| B. | 将2.3g Na投入到97.7g中充分反应,所得溶液中溶质的质量分数为4.0% | |
| C. | 在t℃时,将a g NH3完全溶于水,得到V mL溶液.该溶液的物质的量浓度为$\frac{1000a}{17V}$mol•L-1 | |
| D. | 1mol•L-1的硫酸溶液中c(H+)=1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
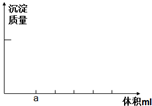 把1.71克硫酸铝配成100ml溶液,为了抑制水解,在配置过程中加入少量硫酸.若在上述溶液中逐滴加入0.5mol/L的氢氧化钠溶液,直至过量.用图象记录滴加过程中产生沉淀的过程.
把1.71克硫酸铝配成100ml溶液,为了抑制水解,在配置过程中加入少量硫酸.若在上述溶液中逐滴加入0.5mol/L的氢氧化钠溶液,直至过量.用图象记录滴加过程中产生沉淀的过程. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com