
 Na2S2O3����Ҫ�Ļ���ԭ�ϣ�������ˮ�������Ի���Ի������ȶ���
Na2S2O3����Ҫ�Ļ���ԭ�ϣ�������ˮ�������Ի���Ի������ȶ������� ��1�����������ˮ�������Ҵ����Ҵ�ʪ�����ʹ������ڷ�ɢ����Һ�У�
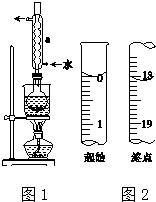
��2������ͼʾװ������������д�������ƣ�Ȼ������������ܹ����������������ý��н��
��3������S2O32?���л�ԭ�ԣ��ױ�������������������ӿ�֪����Ϊ�����ƣ����ݼ�����������ӵķ����������������ƣ�
��4��S2O32?������������Һ���ܹ�����������ԭ��Ӧ�������ʣ��ݴ�д����Ӧ�����ӷ���ʽ��
��5�����ݵζ�ǰ��ҺΪ��ɫ���ζ������ⵥ��ʹ���۱������жϴﵽ�յ�ʱ��Һ��ɫ�仯��
��6������ͼʾ�ĵζ�����Һ��������������ն�����Ȼ���������ĵ�ı���Һ��������ݷ�Ӧ2S2O32-+I2�TS4O62-+2I-��֪��n��S2O32-��=2n��I2����Ȼ��������еⵥ�ʵ����ʵ��������Na2S2O3•5H2O��������Ʒ�Ĵ��ȣ�
��7�����������Ϣ��Na2S2O3��ԭ�Խ�ǿ������Һ���ױ�Cl2������SO42-�������ϼ��������д����Ӧ�����ӷ���ʽ��
��� �⣺��1�����������ˮ���������Ҵ�����������ڷ�Ӧǰ���Ҵ�ʪ����ʹ������ڷ�ɢ����Һ�У�
�ʴ�Ϊ��ʹ������ڷ�ɢ����Һ�У�
��2����������ͼʾװ��ͼ��֪������aΪ�����ܣ���ʵ���������ܾ����������������ã�
�ʴ�Ϊ�������ܣ�����������
��3��S2O32?���л�ԭ�ԣ��ܹ���������������������ӣ����Կ��ܴ��ڵ������������ƣ����������Ƶķ���Ϊ��ȡ������Ʒ���ڹ���ϡ���ᣬ���ˣ�����Һ�м�BaCl2��Һ�����а�ɫ���������Ʒ�к���Na2SO4��
�ʴ�Ϊ��Na2SO4�� ȡ������Ʒ���ڹ���ϡ���ᣬ���ˣ�����Һ�м�BaCl2��Һ�����а�ɫ���������Ʒ�к���Na2SO4��
��4��S2O32?�������ӷ���������ԭ��Ӧ���ɵ���ɫ���ʣ���Ӧ�����ӷ���ʽΪ��S2O32?+2H+=S��+SO2��+H2O��
�ʴ�Ϊ��S2O32?+2H+=S��+SO2��+H2O��
��5���ζ������ⵥ��ʹ���۱��������Եζ��յ�ʱ��Һ��ɫ�仯Ϊ������ɫ��Ϊ��ɫ��
�ʴ�Ϊ������ɫ��Ϊ��ɫ��
��6������ͼʾ�ĵζ�����Һ���֪���ζ����г�ʼ����Ϊ0���ζ��յ�Һ�����Ϊ18.10mL���������ĵ�ı���Һ���Ϊ18.10mL��
���ݷ�Ӧ2S2O32-+I2�TS4O62-+2I-��֪��n��S2O32-��=2n��I2��������W g��Ʒ�к���Na2S2O3•5H2O����Ϊ��0.1000mol•L-1��18.10��10-3L��2��M=3.620��10-3Mg�����Ʒ�Ĵ���Ϊ��$\frac{3.620��1{0}^{-3}Mg}{Wg}$��100%=$\frac{3.620��1{0}^{-3}M}{W}$��100%��
�ʴ�Ϊ��18.10��$\frac{3.620��1{0}^{-3}M}{W}$��100%��
��7��Na2S2O3��ԭ�Խ�ǿ������Һ���ױ�Cl2������SO42-�����ݻ��ϼ����������ƽ������ӷ���ʽΪ��S2O32?+4Cl2+5H2O=2SO42?+8Cl?+10H+��
�ʴ�Ϊ��S2O32?+4Cl2+5H2O=2SO42?+8Cl?+10H+��
���� ���⿼���Ϊ�ۺϣ��漰����ʵ�鷽������ơ�̽�����������������ʺ������к͵ζ������ӷ���ʽ��д��֪ʶ����Ŀ�Ѷ��еȣ���ȷʵ��Ŀ�ġ�ʵ��ԭ��Ϊ���ؼ���ע����������ʵ�鷽�����������ԭ����ȷ̽��������ɵķ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 25��ʱ��pH=13��1.0 L Ba��OH��2��Һ�к��е�OH-��ĿΪ0.2NA | |
| B�� | ��״���£�2.24L Cl2��H2O��Ӧ��ת�Ƶĵ�������Ϊ0.1NA | |
| C�� | �����£�21.0g��ϩ�Ͷ�ϩ�Ļ�������к��е�̼ԭ����ĿΪ1.5NA | |
| D�� | ��״���£�22.4L�״��к��е���ԭ����Ϊ1.0NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
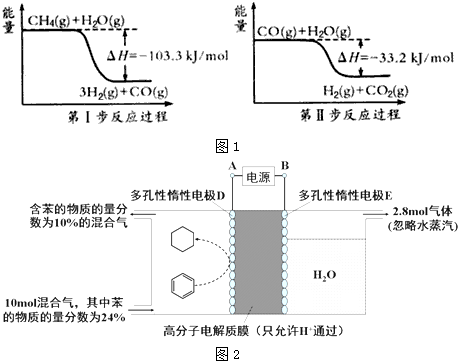
 $?_{����}^{FeSO_{4}/Al_{2}O_{3}}$
$?_{����}^{FeSO_{4}/Al_{2}O_{3}}$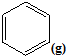 +3H2��g��
+3H2��g���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
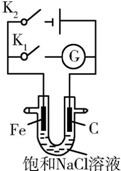
| A�� | K1�պϣ������Ϸ����ķ�ӦΪ2H++2e-�TH2�� | |
| B�� | K1�պϣ�ʯī����Χ��Һ��pH���� | |
| C�� | K2�պϣ��������ᱻ��ʴ�������������������������� | |
| D�� | K2�պϣ���·��ͨ��0.002NA������ʱ������������0.002 mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
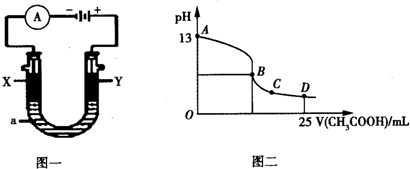
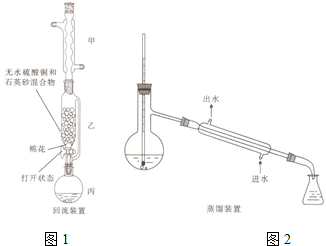 �����ᣨ
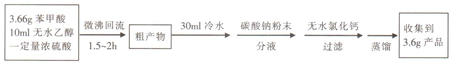
�����ᣨ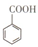 �����Ҵ���Ũ������¿����Ƶñ�������������ʱ��ȥ��Ӧ�в�����ˮ��������IJ��ʣ��ݴ�ijʵ��С�����������ͼ��װ������������ʵ�飮�����Ϣ���£�
�����Ҵ���Ũ������¿����Ƶñ�������������ʱ��ȥ��Ӧ�в�����ˮ��������IJ��ʣ��ݴ�ijʵ��С�����������ͼ��װ������������ʵ�飮�����Ϣ���£�| ��Է������� | �ܶ�/��g•cm-3�� | �е�/�� | ˮ���ܽ�� | |
| ������ | 122 | 1.27 | 249 | �� |
| �Ҵ� | 46 | 0.789 | 78.3 | ���� |
| ���������� | 150 | 1.05 | 212.6 | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʹ��̪���ɫ����Һ�У�Na+��Al3+��SO42-��Cl- | |
| B�� | ��Fe��Ӧ�ܷų�H2����Һ�У�Fe2+��K+��NO3-��SO42- | |
| C�� | $\frac{{K}_{W}}{c��{H}^{+}��}$=1��10-13mol•L-1����Һ�У�NH4+��Ca2+��Cl-��NO3- | |
| D�� | ˮ�����c��H+��=1��10-13mol•L-1����Һ�У�K+��Na+��AlO2-��CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
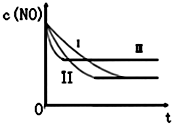 ����β���е���Ҫ��Ⱦ����NO��CO��Ϊ���������Ⱦ���������ͨ�����·�Ӧ����������β����
����β���е���Ҫ��Ⱦ����NO��CO��Ϊ���������Ⱦ���������ͨ�����·�Ӧ����������β����| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| C��NO��10-4 mol/L | 10.0 | 4.50 | C1 | 1.50 | 1.00 | 1.00 |
| C��CO��10-3 mol/L | 3.60 | 3.05 | C2 | 2.75 | 2.70 | 2.70 |
| ʵ�� ��� | T/��C | NO��ʼŨ ��/10-3mol•L-1 | CO��ʼŨ ��/10-3mol•L-1 | �����ı� �����/m2•g-1 |
| �� | 350 | 1.20 | 5.80 | 124 |
| �� | 280 | 1.20 | 5.80 | 124 |
| �� | 280 | 1.20 | 5.80 | 82 |
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ���� ��ʱ��/min | ||
| H2O | CO | CO | H2 | |||
| �� | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
| �� | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
| �� | 900 | a | b | c | d | t |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com