
| A. | 全部 | B. | 除④⑥⑦以外 | C. | ③④⑤⑥ | D. | ②⑤⑥ |
分析 根据价层电子对互斥理论确定微粒空间构型,价层电子对个数=σ键+孤电子对个数,孤电子对个数=$\frac{1}{2}$×(a-xb),a为中心原子的价电子数,x为与中心原子结合的原子个数,b为与中心原子结合的原子最多能接受的电子数,据此判断.
解答 解:①NH3中价层电子对个数=3+$\frac{1}{2}$×(5-3)=4且含有一个孤电子对,所以为三角锥形,H2O中价层电子对个数=2+$\frac{1}{2}$×(6-2)=4且含有两个孤电子对,所以为V形结构,二者空间构型不同,故①错误;
②NH4+中价层电子对个数是4且不含孤电子对,为正四面体形结构;H3O+中O原子价层电子对个数=3+$\frac{1}{2}$(6-1-3×1)=4且含有一个孤电子对,所以为三角锥形结构,二者空间构型不同,故②错误;
③NH3为三角锥形结构、H3O+中O原子价层电子对个数=3+$\frac{1}{2}$(6-1-3×1)=4且含有一个孤电子对,所以为三角锥形结构,所以二者空间构型相同,故③正确;
④O3、SO2中价层电子对个数都是3且都含有一对孤电子对,所以分子空间构型都是V形,故④正确;
⑤CO2分子中价层电子对=σ 键电子对+中心原子上的孤电子对=2+$\frac{1}{2}$(4-2×2)=2,所以二氧化碳是直线型结构,BeCl2中Be价层电子对=σ 键电子对+中心原子上的孤电子对=2+$\frac{1}{2}$(2-2)=2,是sp杂化,是直线型结构,二者空间构型相同,故⑤正确;
⑥NH4+和SO42-中价层电子对个数都是4且不含孤电子对,所以空间构型都是正四面体结构,所以空间构型相同,故⑥正确;
⑦BF3中B原子杂化轨道数=δ键数+孤对电子对数=3+0=3,所以分子构型为平面正三角形,气态氯化铝通常以二聚分子形式存在,Al2Cl6结构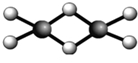 ,Al采用sp3杂化轨道成键,为正四面体结构,二者空间构型不同,故⑦错误;
,Al采用sp3杂化轨道成键,为正四面体结构,二者空间构型不同,故⑦错误;
故选C.
点评 本题考查了微粒空间构型的判断,根据价层电子对理论解答,注意孤电子对个数=$\frac{1}{2}$×(a-xb)中各个字母的含义,气态氯化铝通常以二聚分子形式存在Al采用sp3杂化轨道成键为正四面体结构,为易错点,题目难度中等.


科目:高中化学 来源: 题型:解答题

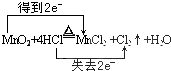 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6:1 | B. | 5:1 | C. | 1:5 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含金属元素的离子都是阳离子 | |
| B. | 在氧化还原反应中,非金属单质一定是氧化剂,金属单质一定是还原剂 | |
| C. | 某元素从化合态变为游离态时,该元素一定被还原 | |
| D. | 金属阳离子被还原不一定得到金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
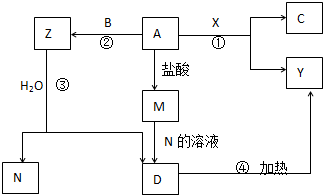 如图转化关系中,A、B、C为单质,其余方框内均为化合物,B、X、N常温下为气体,C为黑色固体,D为白色沉淀,A、Y、Z、M、D中均含同一种元素(框图中某些生成物已略去).请填写下列空白:
如图转化关系中,A、B、C为单质,其余方框内均为化合物,B、X、N常温下为气体,C为黑色固体,D为白色沉淀,A、Y、Z、M、D中均含同一种元素(框图中某些生成物已略去).请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
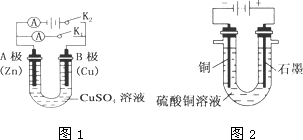 请按要求回答下列问题.
请按要求回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com