
以石墨为电极,电解1L硫酸铜和氯化钠的混合溶液,其中硫酸铜与氯化钠的物质的量之和为0.2mol,硫酸铜的物质的量占总物质的量的比值为x。
(1)若x=0.5,当Cu2+在阴极恰好全部析出时,阳极产生的气体是什么?其物质的量是多少?所得溶液的pH是多少?
⑵电解一段时间后,阴、阳两极产生气体的物质的量恰好相等,均为0.16mol,求此时x的值
Cl2 0.05mol O2 0.025 mol 1 0.6
【解析】(1)若x=0.5,则硫酸铜是0.1mol,氯化钠是0.1mol。阴极首先是铜离子放电,Cu2++2e-=Cu,所以当铜离子放电完毕之后,转移的电子是0.2mol。在阳极上先是氯离子放电,2Cl--2e-=Cl2↑。氯化钠是0.1mol,生成氯气0.05mol,转移电子是0.1mol,所以根据得失电子守恒可知,在阳极上还有氧气生成。因为4OH--4e-=2H2O+O2↑,所以氧气是
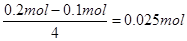 。则同时产生的氢离子是0.1mol,浓度为0.1mol/L,pH是1.
。则同时产生的氢离子是0.1mol,浓度为0.1mol/L,pH是1.
(2)阴、阳两极均产生气体,说明在阴极上当铜离子放电完毕之后,溶液中的氢离子开始放电,2H++2e-=H2↑,氢气是0.16mol,得到电子0.32mol。原混合液中氯化钠最多是0.2mol,即氯离子最多失去0.2mol电子,所以阳极一定还有氧气生成。硫酸铜是0.2xmol,需要得到电子0.4xmol。氯化钠是0.2(1-x)mol。生成氯气是0.1(1-x)mol,则氧气的物质的量是0.16mol-0.1(1-x)mol=(0.06mol+0.1xmol)。根据得失电子守恒可知0.32mol+0.4xmol=0.2(1-x)mol+4×(0.06mol+0.1xmol),解得x=0.6.


科目:高中化学 来源: 题型:
A.以石墨为电极,电解含甲基橙的0.1 mol·L-1硫酸溶液
B.以铜为电极,电解1 mol·L-1硫酸溶液
C.以石墨为电极,电解含酚酞的饱和食盐水
D.以石墨为电极,电解1 mol·L-1溴化钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
A.以石墨为电极,电解含甲基橙的0.1 mol/L硫酸溶液
B.以铜为电极,电解1 mol/L硫酸溶液
C.以石墨为电极,电解含酚酞的饱和食盐水
D.以石墨为电极,电解1 mol/L溴化钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
对下列各溶液进行电解,通电一段时间后,溶液颜色不会发生显著改变的是( )
A.以石墨为电极,电解含甲基橙的0.1 mol·L-1硫酸溶液
B.以铜为电极,电解1 mol·L-1硫酸溶液
C.以石墨为电极,电解含酚酞的饱和食盐水
D.以石墨为电极,电解1 mol·L-1溴化钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源:专项题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com