
| A. | 苯分子中的6个碳原子之间的键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的键 | |
| B. | 一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 | |
| C. | 乙烷和丙烯的物质的量共1 mol,其混合物完全燃烧生成3 mol H2O | |
| D. | 将溴水加入苯中,溴水的颜色变浅,这是由于发生了加成反应 |
分析 A.苯中不含碳碳双键,为平面正六边形;
B.光照下甲基上H被取代,催化剂条件下苯环上H被取代;
C.乙烷和丙烯均含6个H;
D.苯与溴水不反应,发生萃取.
解答 解:A.苯中不含碳碳双键,为平面正六边形,6个碳原子之间的键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的键,故A正确;
B.光照下甲基上H被取代,催化剂条件下苯环上H被取代,则Cl2可在甲苯的苯环或侧链上发生取代反应,故B正确;
C.乙烷和丙烯均含6个H,由H原子守恒可知,乙烷和丙烯的物质的量共1 mol,其混合物完全燃烧生成3 mol H2O,故C正确;
D.苯与溴水不反应,发生萃取,不发生加成反应,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的结构、性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意苯中的化学键,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 | B. | 5 | C. | 6 | D. | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠溶液中:K+、SO42-、Cl-、Al3+ | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=1.0×10-13mol•L-1的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| C. | 与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42- | |
| D. | 有SO42-存在的溶液中:Na+、Mg2+、Ca2+、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 操作 | 现象 |
| 取4g 漂粉精固体,加入100mL 水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH 试纸先变蓝(约为12),后褪色 |
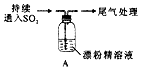 | 1.液面上方出现白雾; 2.稍后,出现浑浊,溶液变为黄绿色; 3.稍后,产生大量白色沉淀,黄绿色褪去 |
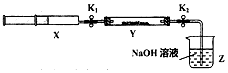
| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中(假设充分反应) | (1)淡黄色固体变为白色粉末 | (2)反应的化学方程式:SO2+Na2O2=Na2SO4 |
| 将注射器活塞退回原处并固定,待装置恢复到室温,打开K2 | (3)Z中NaOH溶液倒吸入Y管中 | (4)不用解释 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ①③④⑤ | C. | ①②③④ | D. | ①②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com