
【题目】已知实验室在加热条件下制取Cl2的化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。现将8.7 g MnO2投入到200 g质量分数为36.5%(过量)的浓盐酸中加热,充分反应后,求:
MnCl2+Cl2↑+2H2O。现将8.7 g MnO2投入到200 g质量分数为36.5%(过量)的浓盐酸中加热,充分反应后,求:
(1)标准状况下生成Cl2的体积。
(2)反应生成的MnCl2的质量为。
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
1 | ① | ||||||
2 | ② | ⑤ | |||||
3 | ③ | ⑥ | |||||
4 | ④ | ⑦ | |||||
(1)表中元素________(填写元素符号)的非金属性最强;元素________(填写元素符号)的金属性最强,写出它与水反应的离子方程式__________________________________。
(2)表中元素③的原子结构示意图是________。
(3)表中元素⑥、⑦氢化物的稳定性顺序为________>________(填写化学式,下同)。
(4)表中元素最高价氧化物对应水化物酸性最强的酸的分子式是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表所示为自然界中的多种铜矿石的主要成分:
矿石名称 | 黄铜矿 | 斑铜矿 | 辉铜矿 | 孔雀石 |
主要成分 | CuFeS2 | Cu5FeS4 | Cu2S | CuCO3Cu(OH)2 |
请回答:
(1)上表所列铜化合物中,铜的质量百分含量最高的是(填化学式)
(2)工业上以黄铜矿为原料.采用火法溶炼工艺生产铜.该工艺的中间过程包含反应: 2Cu2O+Cu2S ![]() 6Cu+SO2↑,则该反应的氧化剂与还原剂的物质的量之比是
6Cu+SO2↑,则该反应的氧化剂与还原剂的物质的量之比是
(3)火法溶炼工艺生产铜的尾气直接排放到大气中造成环境污染的后果是;处理该尾气可得到有价值的化学品,写出其中一种酸和一种盐的名称或化学式、 .
(4)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是(填字母).
选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
A | 铜绿的主成分是碱式碱酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对;有 |
B | 铜表易形成致密的氧化膜 | 铜容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
C | 铁比铜活泼 | 铆在铜板上的铁钉在潮湿空气中不易生锈 | Ⅰ对;Ⅱ对;有 |
D | 蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 | 硫酸铜溶液可用作游泳池的消毒剂 | Ⅰ错;Ⅱ对;无 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为2AgCl+Mg= Mg2++2Ag+2Cl-,有关该电池说法错误的是
A.镁为电池负极B.有24g镁被氧化时,还原得到216g银
C.正极反应为Ag++e-=AgD.可用于海上应急照明
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气根据成分不同分为贫气和富气,贫气中甲烷的含量较多,富气中乙烷、丙烷、丁烷的含量相对高一些.若要将它们液化,下列说法正确的是( )
A.贫气易液化
B.富气易液化
C.二者液化条件相同
D.加压降温均有利于两者液化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生下列反应aA(g) ![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
A. A的转化率变大
B. 平衡向正反应方向移动
C. D的体积分数变大
D. a < c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4HCO3是一种离子化合物,下列关于该物质的叙述错误的是( )
A.所含四种元素的原子半径由小到大的顺序为:H<O<N<C
B.同周期的三种元素的得电子能力由大到小的顺序为:O>N>C
C.与足量烧碱溶液共热的离子方程式为:NH4++OHˉ ![]() NH3↑+H2O
NH3↑+H2O
D.除去NaCl固体中混有少量的NH4HCO3固体可以采用加热的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G均为有机物,其中A 常用来衡量一个国家石油化工发展水平的标志性物质,它们之间有如下转化关系.已知醛基在氧气中易氧化成羧基,请回答下列问题: 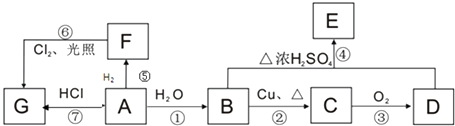
(1)A、B中官能团的名称:A、B;
(2)在F的同系物中最简单的有机物的空间构型为;
(3)写出与F互为同系物的含5个碳原子的所有同分异构体中一氯代物种类最少的结构简式;
(4)写出下列编号对应反应的化学反应方程式,并注明反应类型: ②、反应;
④、反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,A、B反应生成C和D,在2L的密闭容器中进行,起始时加入了4molA和2molB,经过一段时间达到反应限度,测得C的浓度为1mol/L,D的平均反应速率为0.2 mol·L-·min-,A与B都反应了50%,且D与A的化学计量数相同,请回答下列问题:
(1)达到反应限度这段时间内A的反应速率为______________。
(2)写出该反应的化学方程式:________________________________。
(3)达到化学反应限度所用的时间为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com