
ʵ���ҴӺ����Һ����H2O�⣬������CCl4��I2��I�����л��յ⣬��ʵ�������ͼ1��
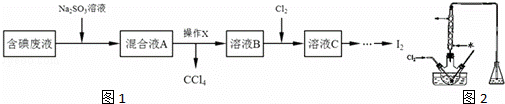
��1�����Һ�м����Թ�����Na2SO3��Һʱ���������ӷ���ʽΪ�������ò�����Ŀ����������
��2������XӦ��������д��������ͼ2���н��У������õ���ҺB�Ĺ��̣��������Һ���ú�����
��3��������ƿ�н���ҺB���������pHԼΪ2������ͨ��Cl2����40˚C���ҷ�Ӧ��ʵ��װ������ͼ��ʾ����ʵ������ڽϵ��¶��½��е�ԭ����������ƿ��ʢ�ŵ���ҺΪ�����������ʵĻ�ѧʽ����
��4��ij�����ˮ��pHԼΪ4����һ������I2�����ܴ���I����IO3��������ʹ�������������ʵĻ�ѧʽ����ͬ����Һ������ܴ��ڵ�I����������Һ������ܴ��ڵ�IO3�����ڼ���ú����ˮ���Ƿ���I����IO3��ǰ����Ҫ���еIJ���������������ţ���
a��ȡ���������ˮ��CCl4�����ȡ����Һ
b����NaOH��Һ����Һ���ڵ�����
c������Һ�е�������������Һ��
| ���ʷ�����ᴿ�ķ����ͻ��������ۺ�Ӧ�ã� | |
| ר�⣺ | ʵ������⣮ |
| ������ | ��1������������ԣ������������������������ƣ���������ԭ���ɵ⣻�ⲻ��������ˮ����������������ˮ�� ��2�����뻥�����ܵ�Һ����÷�Һ�ķ������룬��Ϸ�ũҵʵ�������������ش�õ���Һ�ķ����� ��3���������������������ܽ�������¶ȵ����߶���С�����������������ܺ�����������Һ��Ӧ���������ʣ� ��4�������Ӿ��л�ԭ�ԣ��ܱ��������������ɵ⣬��������Ӿ��������ԣ��ܱ���ԭ����ԭ���ɵ⣬����������Һ����ɫ�� |
| ��� | �⣺��1������������ԣ������������������������ƣ���������ԭ���ɵ⣬���ӷ�Ӧ����ʽΪSO32��+I2+H2O=2I��+2H++SO42�����ⲻ��������ˮ����������������ˮ��Ϊ��ʹ�����IԪ�ؽ���ˮ��ҺӦ���ԭΪ�����ӣ� �ʴ�Ϊ��SO32��+I2+H2O=2I��+2H++SO42����ʹ���Ȼ�̼�еĵ����ˮ�㣻 ��2�����Ȼ�̼�����л��ˮ����������߲����ܣ����뻥�����ܵ�Һ����÷�Һ�ķ������룬���Է�������Ȼ�̼���÷�Һ�ķ�����ʵ������Ϊ��Һ©�����õ���Һ�IJ���Ϊ���������Һ���ú�Һ©���ϲ����ӣ������������ų��²�Һ�壮���²�Һ����ȫ����رջ��������ϲ�����ʣ��Һ�壻 �ʴ�Ϊ����Һ©�����������Һ���ú�Һ©���ϲ����ӣ������������ų��²�Һ�壮���²�Һ����ȫ����رջ��������ϲ�����ʣ��Һ�壻 ��3���������������������ܽ�������¶ȵ����߶���С���¶�Խ�ߣ��������ܽ��ԽС����ӦԽ����֣�����Ӧ���ڵ��������½��з�Ӧ�����������������ж�������ֱ���ſգ��Ҷ��ܺ�����������Һ��Ӧ���������ʣ�������NaOH��Һ���������͵������� �ʴ�Ϊ��ʹ��������Һ���нϴ���ܽ�ȣ����ֹ���������ֹ���һ������������NaOH��Һ�� ��4�������Ӿ��л�ԭ�ԣ��ܱ��������������ɵ⣬��������Ӿ��������ԣ��ܱ���ԭ����ԭ���ɵ⣬����������Һ����ɫ����������鷽��Ϊ�� ��ˮ��ȡ������Һ������1��2mL������Һ�����������ữ���μ�FeCl3��Һ��2I��+2Fe3+=2Fe2++I2������Һ����ɫ��˵����ˮ�к���I��������I���� ����ˮ��ȡ������Һ������1��2mL������Һ���������ữ���μ�Na2SO3��Һ��5SO32��+2 IO3��+2H+=I2+5SO42��+H2O������Һ����ɫ��˵����ˮ�к���IO3��������IO3�����ڼ���ú����ˮ���Ƿ���I����IO3��ǰ����Ҫ���еIJ�����ȡ���������ˮ��CCl4�����ȡ����Һ������Һ�е�������������Һ�����Ƿ������֤���ӵĴ��ڣ� �ʴ�Ϊ��FeCl3 ��Na2SO3��ac�� |
| ������ | ���������ʵ��Ʊ�Ϊ���忼����������ԭ��Ӧ�����ӵļ��顢���ʵķ�����ᴿ����ȷ���ʵ������ǽⱾ��ؼ����������ʵ��������ʡ�����������ᴿ������ѡȡ�ȷ������������֪����ļ��鷽������Ŀ�Ѷ��еȣ� |
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ڸ������������ܴ���������ǣ�������
| �� | A�� | ������ˮ�У�Cl﹣��NO3﹣��Na+��SO32﹣ |
| �� | B�� | �����£� |
| �� | C�� | 0.1 mol/L��NaOH��Һ�У�K+��AlO2﹣��SO42﹣��CO32﹣ |
| �� | D�� | ��PH=7����Һ�У�Fe3+��Na+��Br﹣��Cl﹣ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�绯ѧ���о���ͻ�ѧ��Ӧ���ϵ�Ŀ�ѧ����ء���ⶼ����������֪�ĵ绯ѧ��Ӧ��
��1����ͼ1��һ�ֳ�����һ��п�����Ըɵ�أ��ɵ�ع���ʱ�������ϵĵ缫��Ӧʽ�ǣ�������
MnO2�������dz�ȥ�����ϵ���������������Mn2O3���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�������
��2����̼��Ϊ�缫����Ȼ�ͭ��Һʱ��������̼���ϳ����к�ɫ���������⣬����������ɫ����������
��֪ͭ�Ļ��������ɫ���������£�
| ���� | ��ɫ������ | ���� | ��ɫ������ | |
| ������ͭCu��OH��2 | ��ɫ���岻����ˮ | ����ͭ��CuSO4�� | ��Һ����ɫ | |
| ������ͭ��Cu2O�� | ��ɫ���岻����ˮ | �Ȼ�ͭ��CuCl2�� | ��Һ��ɫ��ϡ��Һ��ɫ | |
| �Ȼ���ͭ��CuCl�� | ��ɫ���岻����ˮ | ��ʽ�Ȼ�ͭ | ��ɫ���岻����ˮ |
ȡ���CuCl2��Һ�������̼�������ϴ�ӡ����������ͼ2װ�ý���ʵ�飬��֤�������
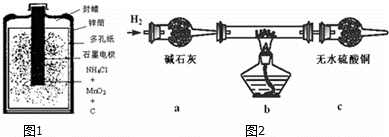
ʵ�������̼���ϵİ�ɫ���ʱ�Ϊ��ɫ����ˮ����ͭ����ɫ��
��̼���ϵĺ�ɫ��������Cu2O����������С����ޡ��������Ҫ˵�������ɣ�������
����cװ�ú�����ͨ����������Һ�У����ְ�ɫ������˵�����ݱ��������Ʋ������̼���ϵ�������ɫ����һ�����ڣ���д������װ��b�з�����Ӧ�Ļ�ѧ����ʽ��������
��������ʵ�������֪�����CuCl2��Һ�������Ϸ����ĵ缫��ӦʽΪ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪25��ʱij��Һ�к��д���Na+��H+��Fe3+��HC03����OH����I���еļ��֣�����ˮ �������c��H+��=1��lO��13 mol/L���������Һ�л���ͨ��һ������Cl2����Һ����ɫ ��Ϊ��ɫ�������йط�����ȷ���ǣ�������
| �� | A�� | ��Һ��pH=1��13 | B�� | ��Һ��һ��û��Fe3+��Na+ |
| �� | C�� | ��Һ����������I��������ȷ��HCO3�� | D�� | ��Cl2������������Һֻ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
˫����ͨ���з���2NO2⇌N2O4+Q��Q��0������ͬʱ�����ձ��зֱ������¡������������ˮ����0.1mol/L H2O2��Һ���ң��������Ҳ��ձ��м�������Fe2��SO4��3������������й��ƶ�����ȷ���ǣ�������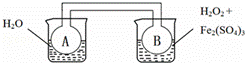
| �� | A�� | ʵ��ʱ��A��B�е�ѹǿʼ����� |
| �� | B�� | ���Ҳ��ձ��������ȷ�Ӧ����A�и���ﵽƽ�� |
| �� | C�� | ���Ҳ��ձ��������ȷ�Ӧ����A����ɫ���� |
| �� | D�� | ���ø�װ���ƶ��Ҳ��ձ��з�Ӧ����ЧӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ࡢ֬���͵�������ά����������������������Ӫ�����ʡ�����������ȷ���ǣ� ��
A��ֲ���Ͳ���ʹ��ˮ��ɫ B������ˮ������ղ�����������
C�������ǡ����Ƕ���ˮ�� D����������Һ�еμ����ṯ��Һ��ɷ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л���������У��ں˴Ź�������ͼ���ܸ��������źŶ��ҷ�ֵ��Ϊ3:2:3����( )
A���������� B����ͪ C������屽 D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ���������ȷ���� _��
A���ڴ������ڵ������£� ������ˮ������Ӧ��������ɫ����ˮ�ص�Һ���屽
B����ͭ˿�������״���ھƾ����ϼ��ȱ�ں���������ʢ����ˮ�Ҵ����Թ��У�����Ҵ�����Ϊ��ȩ��ʵ��
C���Ҵ��к�������ˮ�ɼ�����ʯ���������Ƶ���ˮ�Ҵ�
D���Թ����ȼ���һ����Ũ���ᣬ�����μ������������ᡢ��ˮ�Ҵ���Ȼ�������ȡ��������
E��ʵ������ȡ��ϩʱ�����뼸Ƭ���Ƭ���Ա�����Һ�����ȷ���ʱ��������
F������������Һʱ����ϡ��ˮ����������������Һ�У���������������μӵ������պ��ܽ�Ϊֹ
G����֤������ˮ�����ʱ���������������������Һ��ϣ��������Һ�����á���Һ��ֲ�μ���������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���У���ȷ���ǣ� ��
A. ���õ���ˮ�����Ƶ���ˮ������ʹ��ɫ������ɫ
B. ������Һ�Ⱥ���ˮ��ͬһ������
C. �⻯����Һ�мӵ�����Һ����ɫ
D. �ӵ��ξ�����ʳ���м��������ĵ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com