
【题目】已知 A 的产量通常用来衡量一个国家的石油化工水平,现以 A 为主要原料合成高分子化合物 E 和一种具有果香味的物质 F,其合成路线如下图所示。
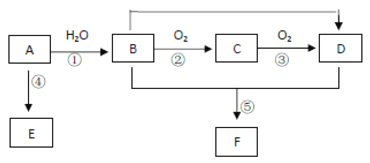
回答下列问题:
(1)工业上由石蜡制取 A 的方法称作: ____________________。
(2)反应⑤的化学方程式:______________________________。
(3)下列有关 A 和 E 的叙述正确的是__________。
a.均能使溴水褪色 b.均只含极性键 c.最简式相同 d.均属于纯净物
![]() (4)写出由 B、O2 和 KOH 溶液组成的燃料电池的负极反应式:____________________。
(4)写出由 B、O2 和 KOH 溶液组成的燃料电池的负极反应式:____________________。
【答案】(1)裂解
(2) CH3COOH+ CH3CH2OH ![]() CH3COOCH2CH3 + H2O
CH3COOCH2CH3 + H2O
(3)c
(4)C2H5OH - 12e- + 16OH- = 2CO32- + 11H2O
【解析】
试题分析:A的产量是衡量一个国家石油化工生产水平的标志,则A是乙烯。乙烯含有碳碳双键,能和水发生加成反应生成乙醇,即B是乙醇。乙醇发生催化氧化生成乙醛,则C是乙醛。乙醛氧化生成乙酸,则D是乙酸,乙醇和乙酸发生酯化反应生成乙酸乙酯,F为乙酸乙酯,以乙烯主要原料合成高分子化合物 E,则E是聚乙烯。
(1)工业上由石蜡制取乙烯的方法叫裂解。
(2)反应⑤是乙酸与乙醇在浓硫酸作催化剂加热的条件发生反应生成乙酸乙酯,反应的化学方程式为:CH3COOH+ CH3CH2OH ![]() CH3COOCH2CH3 + H2O 。
CH3COOCH2CH3 + H2O 。
(3)根据上述分析,A为乙烯,E为聚乙烯,乙烯中含有碳碳双键,而聚乙烯中只有碳碳单键,只有乙烯能使溴水褪色,a项错误;它们有C-C非极性键,b项错误;最简式均为CH2,最简式相同,c项正确;乙烯是纯净物,而聚乙烯属于混合物,d项错误;答案选c。
(4)由 乙醇、O2 和 KOH 溶液组成的燃料电池中,乙醇失电子发生氧化反应生成CO2和水,生成的二氧化碳与KOH反应生成碳酸钾,所以该电池的负极反应式:C2H5OH - 12e- + 16OH- = 2CO32- + 11H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列有关油脂的叙述中,错误的是
A.油脂分子结构中三个烃基一定相同
B.可以用纯碱溶液去除油污
C.可以用纯碱区别植物油和柴油
D.工业上可用油脂制造高级脂肪酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质的操作中错误的是
A.除去石英中少量的碳酸钙:用稀盐酸溶解后过滤
B.FeCl2溶液中混有的FeCl3:加入过量的铁粉充分反应后过滤
C.除去氢氧化铁胶体中的铁离子用渗析的方法
D.氯气混有少量氯化氢气体:将混合气体通过盛NaOH溶液的洗气瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S2O3俗称大苏打(海波)是重要的化工原料。用Na2SO3和硫粉在水溶液中加热反应,可以制得Na2S2O3。已知10℃和70℃时,Na2S2O3在100g水中的溶解度分别为60.0g和212g。常温下,从溶液中析出的晶体是Na2S2O3·5H2O。
现实验室欲制取Na2S2O3·5H2O晶体(Na2S2O3·5H2O的分子量为248)步骤如下:
①称取12.6g Na2SO3于烧杯中,溶于80.0mL水。
②另取4.0g硫粉,用少许乙醇润湿后,加到上述溶液中。
③(如图所示,部分装置略去),水浴加热,微沸,反应约1小时后过滤。
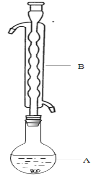
④滤液在经过 、 后析出Na2S2O3·5H2O晶体。
⑤进行减压过滤并干燥。
(1)仪器B的名称是________。其作用是___________。加入的硫粉用乙醇润湿的目的是 。
(2)步骤④应采取的操作是 、 。
(3)滤液中除Na2S2O3和可能未反应完全的Na2SO3外,最可能存在的无机杂质是 。如果滤液中该杂质的含量不很低,其检测的方法是: 。
(4)为了测产品的纯度,称取7.40g 产品,配制成250mL溶液,用移液管移取25.00mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为0.0500mol/L 的碘水,用 (填“酸式”或“碱式”)滴定管来滴定(2S2O32- + I2 = S4O62- + 2I-),滴定结果如下:
滴定次数 | 滴定前读数(mL) | 滴定滴定后读数(mL) |
第一次 | 0.30 | 31.12 |
第二次 | 0.36 | 31.56 |
第三次 | 1.10 | 31.88 |
则所得产品的纯度为 ,你认为影响纯度的主要原因是(不考虑操作引起误差) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修5 有机化学基础】
某抗结肠炎药物有效成分的合成路线如下(部分反应略去试剂和条件):
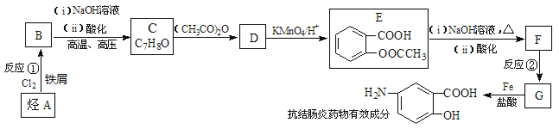
已知: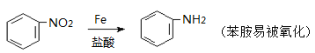
请回答下列问题:
(1)抗结肠炎药物有效成分的分子式是: ;烃A的名称为: ;反应②的反应类型是: 。
(2)①下列对该抗结肠炎药物有效成分可能具有的性质推测正确的是: ;
A.水溶性比苯酚好
B.能发生消去反应也能发生聚合反应
C.1mol该物质最多可与4mol H2发生反应
D.既有酸性又有碱性
② E与足量NaOH溶液反应的化学方程式是: 。
(3)符合下列条件的抗结肠炎药物有效成分的同分异构体有______种。
A.遇FeCl3溶液有显色反应
B.分子中甲基与苯环直接相连
C.苯环上共有三个取代基
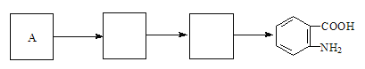
(4)已知:苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位,据此按先后顺序写出以A为原料合成邻氨基苯甲酸(![]() )合成路线中两种中间产物的结构简式(部分反应条件已略去)
)合成路线中两种中间产物的结构简式(部分反应条件已略去)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2离子化合物。
(1)写出Y2O2的电子式:_________________,其中含有的化学键是_______________。
(2)用电子式表示Y2O的形成过程:____________________________________。
(3)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中某区域的一些元素多用于制造半导体材料,它们是( )
A. 稀有气体元素
B. 左下方区域的金属元素
C. 右上方区域的非金属元素
D. 金属元素和非金属元素分界线附近的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由反应物X转化为Y和由反应物X转化为Z的能量变化如图所示。下列说法正确的是
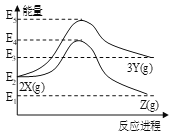
A. 2X(g)![]() 3Y(g)反应的ΔH=E5E2
3Y(g)反应的ΔH=E5E2
B. 2X(g)![]() Z(g)反应的ΔH<0
Z(g)反应的ΔH<0
C. 增大压强有利于提高Y的产率
D. 升高温度有利于提高Z的产率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素的同位素![]() ,它的氯化物XCl21.11g溶于水配成溶液后,加入1mol/L的AgNO3溶液20mL,恰好完全反应生成AgCl沉淀。。已知此核素的原子核内有20个中子,求:
,它的氯化物XCl21.11g溶于水配成溶液后,加入1mol/L的AgNO3溶液20mL,恰好完全反应生成AgCl沉淀。。已知此核素的原子核内有20个中子,求:
(1)X的质量数是多少?。
(2)指出X元素在周期表中的位置。
(3)把少量X的单质放入水中,有何主要现象?写出有关化学方程式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com