
下列方程式书写正确的有
①向NaAlO2溶液中通入过量的CO2:2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32-
②向酸性KMnO4溶液中滴加适量H2C2O4溶液,原溶液紫色褪去:2MnO4-+5H2C2O4=2Mn2-+10CO2↑+2H2O+6OH-
③碳酸的电离方程式:H2CO3 2H++CO32-
2H++CO32-
④NaClO溶液中CIO-的水【解析】
CIO-+H2O=HClO+OH-
⑤酸性条件下,用H2O2将I-氧化为I2:H2O2+2I-+2H+=I2+2H2O
⑥向NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
A. 1个 B. 2个 C. 3个 D. 4个
科目:高中化学 来源:2017届河北省石家庄市高三下学期模拟联考理科综合化学试卷(解析版) 题型:选择题
下列的叙述不正确的是( )
A. 明矾可作净水剂,向海水中加入明矾可以使海水淡化
B. 离子交换膜在工业上应用广泛,在氯碱工业中使用阳离子交换膜
C. 硬币材质一般都是合金.所有的不锈钢中都含有非金属元素
D. 使用含钙、镁离子浓度较大的地下水洗衣服,肥皂去污能力会减弱
查看答案和解析>>
科目:高中化学 来源:山东省2016-2017学年高一3月月考化学试卷 题型:填空题
有A、B、C、D四种元素,它们的原子序数依次增大,由B、C、D形成的离子具有相同的电子层结构。C、D单质都能跟水剧烈反应,lmolC单质跟水反应产生11.2L(标准状况下)B气体单质,1 mol D单质跟水反应产生11.2 L(标准状况下)A气体单质,此时D转化成具有氖原子核外电子层结构的离子。试填空:
(1)这四种元素的名称为A_______,B_______,C_______,D_______。
(2) C原子的结构示意图为_______,D离子的结构示意图为_______。
(3)这四种元素的原子半径由小到大的顺序为_______(用元素符号来表示)。
(4)写出C、D单质分别与水反应的化学方程式:
D+H2O:________________;D+H2O:________________。
(5)从以上两个反应中,判断B和C单质的氧化性:
_______>_______,A和D单质的还原性:_______> _______ (填化学式)。
查看答案和解析>>
科目:高中化学 来源:山东省2016-2017学年高一3月月考化学试卷 题型:选择题
下列有关表述错误的是( )
A. IBr的电子式: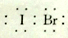
B. HClO的结构式为H-O-C1
C. HIO各原子都满足8电子结构
D. CaF2的形成过程可以表示为: 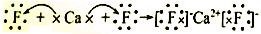
查看答案和解析>>
科目:高中化学 来源:2017届陕西省咸阳市高三二模理综化学试卷(解析版) 题型:填空题
1.
纳米级Cu2O由于具有优良的催化性能而备受关注,下表为制取纳米级Cu2O的三种方法:
窗体顶端
方法Ⅰ | 用炭粉在高温条件下还原CuO |
方法Ⅱ | 电解法,反应为2Cu+H2O |
方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是反应条件不易控制,若控温不当易生成________而使Cu2O产率降低。
(2)已知:2Cu(s)+1/2O2(g)=Cu2O(s) △H =-akJ·mol-1
C(s)+1/2O2(g)=CO(g) △H =-bkJ·mol-1
Cu(s)+1/2O2(g)=CuO(s) △H =-ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)= Cu2O(s)+CO(g);△H =_____。
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,电解装置如下图所示。
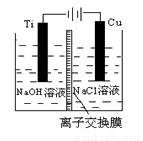
①阴极上的产物是________ 。
②阳极生成Cu2O,其电极反应式为_________。
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2,该反应的化学方程式为____________。
(5)肼又称联氨,易溶于水,是与氨类似的弱碱,用电离方程式表示肼的水溶液显碱性的原因______。
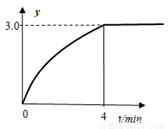
(6)向1L恒容密闭容器中充入0.1molN2H4,在30℃、Ni-Pt催化剂作用下发生反应N2H4(g) N2(g)+2H2(g),测得混合物体系中,
N2(g)+2H2(g),测得混合物体系中,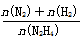 (用y表示)与时间的关系如图所示。0-4min时间内H2的平均生成速率v(H2)=____mol/(L·min);该温度下,反应的平衡常数=_______。
(用y表示)与时间的关系如图所示。0-4min时间内H2的平均生成速率v(H2)=____mol/(L·min);该温度下,反应的平衡常数=_______。
(7)肼-空气清洁燃料电池是一种碱性燃料电池,电解质溶液时20%-30%的KOH溶液。肼-空气燃料电池放电时,负极的电极反应式是_________。电池工作一点时间后,电解质溶液的pH将_______(填“增大”、“减小”、“不变”)。
查看答案和解析>>
科目:高中化学 来源:2017届四川省南充市高三第二次高考适应性考试理综化学试卷(解析版) 题型:填空题
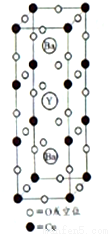
1911年,科学家发现汞在4.2K以下时电阻突然趋近于零——即低温超导性。1986年,科学家又发现了Nb3Ge在23K下具有超导性。1987年2月,赵忠贤及合作者独立发现了在液氮温区(沸点77K)的高温超导体,其晶胞如图所示,元素组成为Ba-Y-Cu-O(临界温度93K),推动了国际高温超导研究。赵忠贤院士获得2016年度国家最高科学技术奖。
(1)汞位于第六周期,且与锌同族,写出Hg的最外层电子排布式________。
(2)Ge元素属于_____(从下列选项中选择)
A.s区 B.类金属 C.非金属 D.过渡金属 E.准金属
(3)Ge(CH3)2Cl2分子的中心原子Ge的杂化方式是________
(4)NH3也常作制冷剂,其分子构型是______,NH3的沸点(239.6℃)高于N2沸点的主要原因是_____
(5)图示材料的理想化学式(无空位时)为_____,若Y(钇)元素的化合价为+3,则Cu的平均化合价为___
(6)金属铜为立方晶胞,空间利用率为74%,晶胞边长为a cm,铜的相对原子质量为63.5,阿伏伽德罗常数为NA。则金属铜的晶体密度ρ=_____g/cm3(只含一个系数,用a、NA表示)
查看答案和解析>>
科目:高中化学 来源:2017届四川省南充市高三第二次高考适应性考试理综化学试卷(解析版) 题型:选择题
利用下图装置可以进行实验并能达到实验目的的是
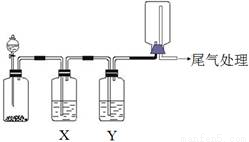
选项 | 实验目的 | X中试剂 | Y中试剂 |
A | 用MnO2和浓盐酸制取并收集纯净干燥的Cl2 | 饱和食盐水 | 浓硫酸 |
B | 用Cu与稀硝酸制取并收集纯净干燥的NO | 水 | 浓硫酸 |
C | 用CaO于浓氨水制取并收集纯净干燥的NH3 | NaOH溶液 | 碱石灰 |
D | CaCO3和稀盐酸制取并收集纯净干燥的CO2 | 饱和NaHCO3溶液 | 浓硫酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 铅蓄电池充电时,阳极质量增大
B. 0.1mol ·L-lCH3COONa溶液加热后,溶液的pH减小
C. 标准状况下,11.2L苯中含有的碳原子数为3×6.02×1023
D. 室温下,稀释0.1mol·L-1氨水,c(H+)·c(NH3·H2O)的值减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省西安市高二下学期第一次教学检测化学试卷(解析版) 题型:选择题
两种气态烃的混合物共1 L,在空气中完全燃烧得到1.5 L CO2和2 L水蒸气(体积均在同温同压下测定),关于此混合烃的判断正确的是( )
A. 两种烃分子中氢原子数都是4 B. 肯定是甲烷和乙烯的混合物
C. 一定不是甲烷和乙烯的混合物 D. 一定含乙烯,不含甲烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com