
 如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:分析 (1)依据C=$\frac{1000ρω}{M}$计算硫酸的物质的量浓度;
(2)依据配制溶液体积选择容量瓶规格,依据浓硫酸稀释过程中溶质的物质的量不变计算需要浓硫酸体积;
(3)根据配制一定物质的量浓度的溶液的步骤对各操作进行排序;
(4)根据c=$\frac{n}{V}$可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量n和溶液的体积V引起的,误差分析时,关键要看配制过程中引起n和V怎样的变化:若n比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若n比理论值大,或V比理论值小时,都会使所配溶液浓度偏大.
解答 解:(1)浓硫酸试剂瓶上的标签,依据C=$\frac{1000ρω}{M}$可知该浓硫酸的物质的量浓度C=$\frac{1000×1.84×98%}{98%}$=18.4mol/L;
故答案为:18.4;
(2)配制480 mL物质的量浓度为0.1 mol•L-1稀硫酸,需要选择500mL容量瓶,实际配制500mL溶液,设需要浓硫酸体积为V,则依据浓硫酸稀释过程中溶质的物质的量不变得:V×18.4mol/L=0.1mol/L×500mL,解得V=2.7mL;
故答案为:2.7;
(3)配制500mL 0.1mol/L的稀硫酸溶液的步骤为:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,所以正确的顺序为:BCAFED;
E定容时改用胶头滴管加蒸馏水,使溶液凹面最低处恰好与刻度线相切;
故答案为:BCAFED;胶头滴管;
(4)A.摇匀后静置,发现液面低于刻线,继续加水至与刻线相切,导致溶液体积偏大,溶液浓度偏低,故A不选;
B.量取浓硫酸时俯视读数,导致量取的硫酸的物质的量偏小,溶液浓度偏低,故B不选;
C.定容时仰视读数,导致溶液体积偏大,溶液浓度偏低,故C不选;
D.在配制前用己知浓度的稀硫酸润洗容量瓶,导致溶质硫酸的物质的量偏大,溶液浓度偏高,故D选;
E.洗涤量取浓硫酸的量简,并将洗涤液一并转入烧杯中,导致量取的浓硫酸体积偏大,硫酸的物质的量偏大,溶液浓度偏高,故E选;
F.溶液没有恢复到室温就进行定容,冷却后,液面下降,溶液体积偏小,溶液浓度偏高,故F选;
故选:DEF.
点评 本题考查了配制一定物质的量浓度的溶液的方法,该题是中等难度的试题,侧重对学生能力的培养和解题方法的指导和训练,明确配制原理及操作步骤是解题关键,注意误差分析方法.


科目:高中化学 来源: 题型:选择题
| A. | 该溶液的中水电离出的c(H+)=10-amol/L | |
| B. | 加水稀释,醋酸钠的水解程度增大,水的电离程度也增大 | |
| C. | 加入盐酸,pH=7时,有c(Cl-)=c(CH3COOH) | |
| D. | 向溶液中加入醋酸呈酸性,则一定是c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 | B. | 5 | C. | 6 | D. | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性 | B. | 还原性 | C. | 酸性 | D. | 碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y只能形成一种化合物 | |
| B. | 最高价氧化物对应水化物的酸性:N>M | |
| C. | 单质与水反应的剧烈程度:Z>Y | |
| D. | 气态氢化物稳定性:M>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④③①⑤ | B. | ②③⑤① | C. | ⑥③④① | D. | ⑥③①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
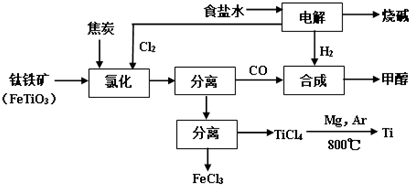
| 物质 | 沸点(℃) |
| TiCl4 | 136 |
| FeCl3 | 315 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O.lmol铁粉与足量水蒸气反应生成的H2分子数目为0.1NA | |
| B. | 分子数目为0.1NA的N2和NH3混合气体,原子间含有的共用电子对数为0.3NA | |
| C. | 电解饱和食盐水时,当阴极产生H2 22.4L时,电路中转移的电子数为2NA | |
| D. | 常温常压下,4.4g乙醛所含σ键数目为0.7NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com