
【题目】氢原子的电子云图中的小黑点表示的意义是( )
A. 一个小黑点表示一个电子 B. 黑点的多少表示电子个数的多少
C. 表示电子运动的轨迹 D. 电子在核外空间出现机会的多少
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
【题目】已知我们所学的烃和烃的衍生物具有下列转化关系,请回答有关问题。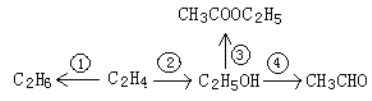
(1)写出以上三个反应的化学方程式(需注明反应所需的条件):
①__________________________________;
②__________________________________;
④__________________________________。
(2)在有机反应类型分类中,反应②属于______________,反应③属于___________。
(3)含有4个碳原子,与C2H6互为同系物的物质的分子式为_____________,写出该组成互为同分异构体的化合物的结构简式__________________,____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,反应2SO2+O2![]() 2SO3,达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8 mol,n(SO3)=1.4 mol,此时SO2的物的量应是( )
2SO3,达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8 mol,n(SO3)=1.4 mol,此时SO2的物的量应是( )
A. 0.4 mol B. 0.6 mol C. 0.8 mol D. 1.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温下,将2molSO2和1mo O2的混合气体通入一个容积固定的5L密闭容器中,发生如下反应:2SO2(g)+O2 (g) ![]() 2SO3 (g)
2SO3 (g)
(1)若2分钟后,测得O2的浓度为0.1mol/L,则2分钟内O2的平均反应速率为____________。
(2)5分钟后反应达平衡,混合气体的物质的量为2.4mol,则平衡时SO3的物质的量为_______________ 。
(3)达平衡时,SO2的转化率为____________ ,平衡时容器内的压强与起始时的压强之比为___________ 。
(4)若平衡后,向该容器中充入一定量的氩气,化学平衡将_____________ 。(正向移动、逆向移动、不移动);若平衡后,向该容器中再充入2molSO2和1molO2,当反应再次达平衡时,SO2的转化率将____________ (增大、减小、不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国药学家屠哟哟因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖。青蒿素结构式如右图所示,下列有关青蒿素研究的说法不正确的是

A. 提取过程中为防止破坏青蒿素结构,应避免高温,故采用低沸点溶剂乙酸进行萃取
B. 可使用质谱仪测出这个分子的相对分子质量,也可用紫外光谱确定这个分子的环状结沟
C. 青蒿素是脂溶性的,既可看作是醚类也可看作是酯类,既有氧化性又有还原性
D. 元索分析仪可以确定青蒿素中是否含有C、H、O等元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下两个反应:(A)NaOH+HCl===NaCl+H2O (B)2FeCl3+Cu===2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)(A)______,(B)________;
(2)如果(A或B)不能,说明其原因_________________________________________;
(3)如果(A或B)可以,则在下面方框中画出装置图并写出正、负极材料及电极反应式
________
负极:________、_______________________________________;
正极:________、________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应C(s) + CO2(g) ![]() 2 CO(g) ΔH > 0,达到平衡状态,现进行如下操作:① 升高反应体系的温度;② 增加反应物C的用量;③ 缩小反应体系的体积;④ 减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的( )
2 CO(g) ΔH > 0,达到平衡状态,现进行如下操作:① 升高反应体系的温度;② 增加反应物C的用量;③ 缩小反应体系的体积;④ 减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的( )
A.①②③④ B.①③ C.④② D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用1 L 1 molL-1 NaOH溶液吸收0.8 mol CO2,所得溶液中Na2CO3和NaHCO3的物质的量之比约为
A. 1∶3 B. 1∶2 C. 2∶3 D. 3∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com