
| A、H2O |
| B、NH3 |
| C、CaCl2 |
| D、CH4 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、在含大量Al3+的溶液中:NH4+、Na+、HCO3-、SO42- |
| B、能使甲基橙试液变红的溶液中:Na+、K+、MnO4-、Cl- |
| C、在水电离出的c(H+)=10-13mol?L-1 的溶液中:NH4+、AlO2-、SO42-、NO3- |
| D、加Al粉能放H2的溶液中:K+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液溴和苯分别受热变为气体 |
| B、干冰和氯化铵分别受热变为气体 |
| C、二氧化硅和铁分别受热熔化 |
| D、食盐和葡萄糖分别溶解在水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 结构或性质信息 |
| T | 基态原子的L层上s电子数等于p电子数 |
| X | 基态原子的最外层未成对电子数在该元素所在周期中最多 |
| Y | 基态原子的第一电离能在该元素所在周期中最小 |
| Z | 单质常温、常压下是气体.基态原子的M层上有1个未成对的p电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
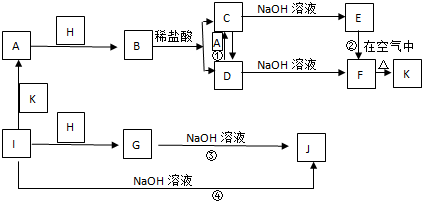
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com