
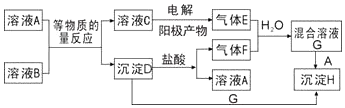
分析 E为黄绿色气体,应为Cl2,F为无色刺激性气味的气体,并且能与E反应,应为SO2,则G应为硫酸和盐酸的混合物,H为BaSO4,A为BaCl2,D为BaSO3,B为Na2SO3,C为NaCl,结合对应物质的性质以及题目的要求可解答该题.
解答 解:E为黄绿色气体,应为Cl2,F为无色刺激性气味的气体,并且能与E反应,应为SO2,则G应为硫酸和盐酸的混合物,H为BaSO4,A为BaCl2,D为BaSO3,B为Na2SO3,C为NaCl,
(1)由以上分析可知E为Cl2,B为Na2SO3,
故答案为:Cl2;Na2SO3;
(2)C→E的反应为电解饱和食盐水的反应,方程式为2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH-,D+G→H的反应为亚硫酸钡和混酸的反应,
反应的离子方程式为BaSO3+2H++SO42-=BaSO4↓+SO2↑+H2O,
故答案为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH-;BaSO3+2H++SO42-=BaSO4↓+SO2↑+H2O;
(3)①E和F发生:Cl2+SO2+2H2O=H2SO4+2HCl,当二者等物质的量反应时生成盐酸和硫酸,溶液呈酸性,滴入几滴石蕊溶液,溶液变红,
故答案为:变红色;Cl2+SO2+2H2O=H2SO4+2HCl;
②如氯气的物质的量大于二氧化硫的物质的量,发生Cl2+H2O=HCl+HClO,滴入几滴石蕊溶液,溶液呈酸性,溶液先变红,但生成次氯酸使溶液褪色,
故答案为:先变红后褪色(或褪色).
点评 本题考查无机物的推断,本题注意以E的颜色、F的气味为推断该题的突破口,熟练掌握相关元素混合物的性质为解答该题的关键,该题很好地考查学生的思维、推断、分析能力,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验台上的易燃、易爆药品要远离火源 | |
| B. | 如果浓硫酸沾到皮肤上应迅速用抹布擦去,再用大量水冲洗,最后涂上小苏打溶液 | |
| C. | 少量碱液滴到实验台上,用湿抹布擦干净,再用水冲洗 | |
| D. | 一旦发现实验室里出现火灾情况,应立即报告学校领导,然后向119报警 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 实验小组用0.50mol/L KOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
实验小组用0.50mol/L KOH溶液和0.50mol/L硫酸溶液进行中和热的测定.| 项目 数据 次数 | 起始温度T1/℃ | 终止温度T2/℃ | 温度差平均值 (T2-T1)/℃ | ||
| H2SO4 | KOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 4.0 |
| 2 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 3 | 26.4 | 26.2 | 26.3 | 30.4 | |
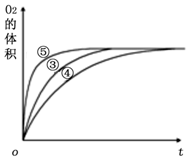
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 10 mL 5% H2O2溶液 | 无 |
| ③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol•L-1 X溶液 |
| ④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol•L-1 X溶液 |
| ⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol•L-1 X溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可逆反应达到平衡状态后,改变外界条件后,若反应速率发生变化,则平衡一定发生移动 | |
| B. | 大多数化学反应在一定条件下都有一定限度 | |
| C. | 使用催化剂可降低反应活化能,加快反应速率,改变反应限度 | |
| D. | FeCl3溶液与KSCN溶液反应达到平衡时,加入少量KCl溶液,因K+、Cl-一直在溶液中存在,所以溶液颜色不会变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原混合气体中O2和CH4的体积比为2:1 | |
| B. | 残留物中只有Na2CO3和NaOH | |
| C. | 反应中电子转移总数为0.8NA | |
| D. | 残留物质量为26.6克 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
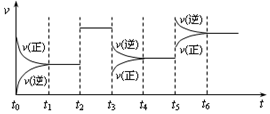
| A. | t2时增加了X的浓度 | B. | t3时增大了压强 | ||
| C. | t5时升高了温度 | D. | t4~t5时间内转化率最大 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1.6gNH2-离子含有的电子数为NA | |
| B. | 20℃、1.0×105Pa时,11.2 L氧气所含的原子数为NA | |
| C. | 标准状况下,2.24LCHCl3含有的共价键数为0.42 NA | |
| D. | 1L 2mol•L-1的硝酸镁溶液中含有的硝酸根离子数为4 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com