
| X | Y | |
| A | 氢氧化钡 | 明矾 |
| B | 醋酸钠 | 醋酸 |
| C | 碳酸氢钠 | 石灰水 |
| D | 氢氧化钠 | 硫酸 |


科目:高中化学 来源: 题型:
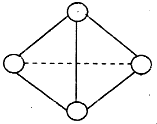 现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E同主族,且D的氢化物常温时为液态.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子.
现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E同主族,且D的氢化物常温时为液态.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子.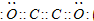
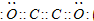
查看答案和解析>>
科目:高中化学 来源: 题型:
表中为一些短周期元素及相应氢化物沸点的数据:
| ||||||||||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
(2012?朝阳区一模)常温时,在X的溶液中先滴入几滴酚酞溶液后变红,再加入等体积的Y的溶液,混合溶液一定显红色的是(溶液物质的量浓度均为0.01mol/L)
|
查看答案和解析>>
科目:高中化学 来源:朝阳区一模 题型:单选题
| X | Y | |
| A | 氢氧化钡 | 明矾 |
| B | 醋酸钠 | 醋酸 |
| C | 碳酸氢钠 | 石灰水 |
| D | 氢氧化钠 | 硫酸 |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com