

分析 (1)根据n=$\frac{m}{M}$计算有机物A、二氧化碳、水的物质的量,根据原子守恒计算烃分子中C、H原子数目,根据相对原子质量计算分子中氧原子数目,据此书写该烃的分子式;
(2)红外光谱分析表明A分子中含有O-H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1,分子中有3种不同的H原子,原子数目之比为6:1:1,结合有机物的分子式判断有机物A的结构;
(3)根据有机物A含有是官能团进行分析解答.
解答 解:(1)有机物A只含有C、H、O三种元素,质谱图表明其相对分子质量为84,16.8g有机物A的物质的量=$\frac{16.8g}{84g/mol}$=0.2mol,经燃烧生成44.0g CO2,物质的量为1mol,生成14.4g H2O,物质的量为 $\frac{14.4g}{18g/mol}$=0.8mol,故有机物A分子中N(C)=$\frac{1mol×1}{0.2mol}$=5,N(H)=$\frac{0.8mol×2}{0.2mol}$=8,故N(O)=$\frac{84-12×5-8}{16}$=1,故A的分子式为C5H8O,
故答案为:C5H8O;
(2)不饱和度为 $\frac{2×5+2-8}{2}$=2,红外光谱分析表明A分子中含有O-H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1,故分子中含有2个CH3、1个-OH连接在同一C原子上,故A的结构简式为 ,
,
故答案为: ;
;
(3)红外光谱分析表明A分子中含有O-H键和位于分子端的C≡C键,不饱和度为 $\frac{2×5+2-8}{2}$=2,不含其它官能团,含有羟基,能与钠反应,含有C≡C双键,能与酸性高锰酸钾发生氧化反应,能与溴发生加成反应,能与氢气发生加成反应,
故答案为:ABCD.
点评 本题考查有机物的推断,为高频考点,涉及有机物分子式及结构式的确定、官能团性质、同分异构体书写等,难度中等,是对学生综合能力的考查,确定分子式是解题的关键.


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:选择题
| A. | H8+x-2yR | B. | H8-x+2yR | C. | Hx-2yR | D. | H2y-xR |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氟酸在玻璃器皿上刻蚀标记 | B. | 液氨用作制冷剂 | ||
| C. | 铁粉作食品袋内的脱氧剂 | D. | 漂粉精作消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
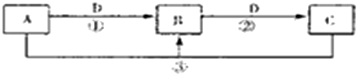
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4 | B. | CH4 | C. | C2H2 | D. | C2H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 纯碱溶液 | 立即产生气泡 |
| B | 氯化铝溶液 | 浓氢氧化钠溶液 | 立即产生白色沉淀 |
| C | 稀盐酸 | 偏铝酸钠溶液 | 立即产生白色沉淀 |
| D | 稀硫酸 | 酸性高锰酸钾溶液 | 溶液逐渐褪色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
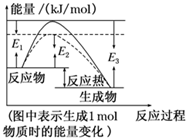 可逆反应N2+3H2?2NH3是工业上合成氨的重要反应.
可逆反应N2+3H2?2NH3是工业上合成氨的重要反应.查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com