
���� ��1����a���Ȼ�ѧ����ʽҪ�������ʵľۼ�״̬�������ʱ�ķ��ź͵�λҪ��ȷ�������Ȼ�ѧ����ʽ����д�������ش�
��b����ϻ�ѧ��Ӧ�ܢݣ����ø�˹�������ش�
��2����Ӧ�Ļ����ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ�����������ͼ��������ϵ��֪���淴Ӧ�Ļ��=����Ӧ�Ļ��+��Ӧ���ʱ䣻
��3����֪��CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��g����H=-574kJ•mol-1����CH4��g��+4NO��g���T2N2��g��+CO2��g��+2H2O��g����H=-1 160kJ•mol-1��
���ø�˹����$\frac{1}{2}$����+�ڣ��ɵã�CH4��g��+2NO2��g���TN2��g��+CO2��g��+2H2O��g������H=-$\frac{574+1160}{2}$kJ•mol-1=867kJ•mol-1�����ݻ��ϼ۱仯�������Ӧ0.2mol����ת�Ƶĵ��������ų���������
��� �⣺��1����a�������Ȼ�ѧ����ʽ����д�������٢ڢ۶����д���ģ�����֮���ֱ��ǣ����С�H=+177.7/mol���ڷ�Ӧ���ȣ���H=+131��KJ/mol���۳�H2O���������ʵ�״̬���ǡ�l��ӦΪ��aq����
�ʴ�Ϊ���٢ڢۣ�
��b����ϻ�ѧ��Ӧ�ܢݣ����ø�˹���ɣ���ӦC��s��+$\frac{1}{2}$O2��g��=CO��g���Ǣ�-�ݵ����������ʱ��H=��-393.5kJ/mol��-��-283kJ/mol��=-110.5KJ/mol��
�ʴ�Ϊ��C��s��+$\frac{1}{2}$O2��g��=CO��g����H=-110.5KJ/mol��
��2����Ӧ�Ļ����ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ�����������ͼ��������ϵ��֪���淴Ӧ�Ļ��=����Ӧ�Ļ��+��Ӧ���ʱ䣻H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=-241.8kJ•mol-1���÷�Ӧ�Ļ��Ϊ167.2kJ•mol-1�������淴Ӧ�Ļ��=167.2KJ/mol+241.8KJ/mol=409.0KJ/mol��
�ʴ�Ϊ��409.0��
��3����֪��CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��g����H=-574kJ•mol-1����CH4��g��+4NO��g���T2N2��g��+CO2��g��+2H2O��g����H=-1 160kJ•mol-1��
���ø�˹����$\frac{1}{2}$����+�ڣ��ɵã���CH4��g��+2NO2��g���TN2��g��+CO2��g��+2H2O��g������H=-$\frac{574+1160}{2}$kJ•mol-1=-867kJ•mol-1��
�����4.48L��������ʵ���Ϊ��n��CH4��=$\frac{4.48L}{22.4L/mol}$=0.2mol��������̼Ԫ�صĻ��ϼ�Ϊ-4�ۣ���Ӧ���������̼��CԪ�ػ��ϼ�Ϊ+4�ۣ����ϼ۱仯Ϊ8������ȫ��Ӧ1mol����ת����8mol��8NA�����ӣ���Ӧ0.2mol����ת�Ƶĵ�������Ϊ��0.2mol��8NA=1.6NA�������Ȼ�ѧ����ʽ�ۿ�֪����ȫ��Ӧ0.2mol������ȵ�����Ϊ��867kJ•mol-1��0.2mol=173.4kJ��
�ʴ�Ϊ��1.6NA��173.4��
���� ���⿼�鷴Ӧ���Լ�������ԭ��Ӧ�ļ��㣬��Ŀ�Ѷ��еȣ�ע�����ո�˹���ɵĺ��弰�Ȼ�ѧ����ʽ����дԭ����ȷ������ԭ��Ӧ�е���ת�Ƶļ��㷽�������������ѧ���ļ��������ͷ��������Ŀ��飮


 �Ͻ�ƽ��У����ϵ�д�
�Ͻ�ƽ��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
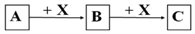
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
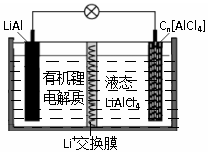 ij�����͵�صĹ���ԭ����ͼ����ʾ��CnΪʯīϩ��Һ̬LiAlCl4�к���Li+��AlCl4-������˵����ȷ���ǣ�������
ij�����͵�صĹ���ԭ����ͼ����ʾ��CnΪʯīϩ��Һ̬LiAlCl4�к���Li+��AlCl4-������˵����ȷ���ǣ�������| A�� | ���ʱ��CnΪ�������缫��ӦΪ��Cn+AlCl4--e-�TCn[AlCl4] | |
| B�� | �ŵ�ʱ������·��ͨ��0.1mol����ʱ����0.1molLi+ͨ������Ĥ��LiAl���ƶ� | |
| C�� | LiAl����ǿ�����ԣ��ŵ�ʱ���������� | |
| D�� | ����п��ܷ�������Ӧ��2Al+6H2O�T2Al��OH��3+3H2�����ʸõ�ش��ڰ�ȫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��̬�⻯������ȶ��ԣ�b��c | B�� | ��dԪ�ص�����Һ���ܳʼ��� | ||
| C�� | ԭ�Ӱ뾶��d��c��b��a | D�� | a��b��c����Ԫ�����γ����ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
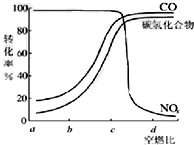 �������ϰ�װ��Ч��ת��������ʹ����β���е���Ҫ��Ⱦ�CO��NOx��̼�⻯����������Ӧ�����������ʣ���������β����Ⱦ��
�������ϰ�װ��Ч��ת��������ʹ����β���е���Ҫ��Ⱦ�CO��NOx��̼�⻯����������Ӧ�����������ʣ���������β����Ⱦ��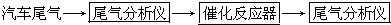
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol�������е�ԭ����ΪNA | |
| B�� | NA��ˮ�����к�����ԭ�ӵ����ʵ���Ϊ2 mol | |
| C�� | 1 mol �����к��еķ�����Ϊ2NA | |
| D�� | 1 mol�κ����ʶ�����NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
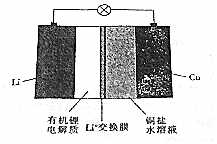
| A�� | �ŵ�ʱ���������н�������� | |
| B�� | ���ʱ����������Һ��c��Cu2+������ | |
| C�� | �ŵ�ʱ����������Һ��c��OH-������ | |
| D�� | ���ʱ�������ĵ缫��ӦʽΪCu2++2e-�TCu |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2Ϊ0.4 mol•L-1��O2Ϊ0.2 mol•L-1 | |
| B�� | SO2Ϊ0.2 mol•L-1 | |
| C�� | SO2��SO3�ֱ�Ϊ0.15 mol•L-1��0.3 mol•L-1 | |
| D�� | SO3Ϊ0.4 mol•L-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com