
”¾ĢāÄæ”æ¼×”¢ŅŅĮ½Ķ¬Ń§ĪŖĢ½¾æ![]() ÓėæÉČÜŠŌ±µµÄĒæĖįŃĪÄÜ·ń·“Ӧɜ³É°×É«BaSO3³Įµķ£¬ÓĆĻĀĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃé£Ø¼Š³Ö×°ÖĆŗĶAÖŠ¼ÓČČ×°ÖĆŅŃĀŌ£¬ĘųĆÜŠŌŅŃ¼ģŃ飩”£
ÓėæÉČÜŠŌ±µµÄĒæĖįŃĪÄÜ·ń·“Ӧɜ³É°×É«BaSO3³Įµķ£¬ÓĆĻĀĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃé£Ø¼Š³Ö×°ÖĆŗĶAÖŠ¼ÓČČ×°ÖĆŅŃĀŌ£¬ĘųĆÜŠŌŅŃ¼ģŃ飩”£
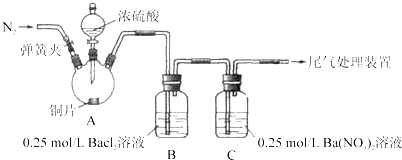
ŹµŃé²Ł×÷ŗĶĻÖĻó£ŗ
²Ł×÷ | ĻÖĻó |
¹Ų±ÕµÆ»É¼Š£¬µĪ¼ÓŅ»¶ØĮæÅØĮņĖį£¬¼ÓČČ | AÖŠÓŠ°×ĪķÉś³É£¬Ķʬ±ķĆę²śÉśĘųÅŻ£¬BÖŠÓŠĘųÅŻĆ°³ö£¬²śÉś“óĮæ°×É«³Įµķ£¬CÖŠ²śÉś°×É«³Įµķ£¬ŅŗĆęÉĻ·ÅĀŌĻŌĒ³×ŲÉ«²¢Öš½„ĻūŹ§ |
“ņæŖµÆ»É¼Š£¬ĶØČėN2£¬Ķ£Ö¹¼ÓČČ£¬Ņ»¶ĪŹ±¼äŗó¹Ų±Õ | |
“ÓB”¢CÖŠ·Ö±šČ”ÉŁĮæ°×É«³Įµķ£¬¼ÓĻ”ŃĪĖį | ÉŠĪ“·¢ĻÖ°×É«³ĮµķČܽā |
(1)AÖŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ_________________”£
(2)CÖŠ°×É«³ĮµķŹĒ_______£¬øĆ³ĮµķµÄÉś³É±ķĆ÷SO2¾ßÓŠ_______ŠŌ”£
(3)CÖŠŅŗĆęÉĻ·½Éś³ÉĒ³×ŲÉ«ĘųĢåµÄ»Æѧ·½³ĢŹ½ŹĒ______”£
(4)·ÖĪöBÖŠ²»ČÜÓŚĻ”ŃĪĖįµÄ³Įµķ²śÉśµÄŌŅņ£¬¼×ČĻĪŖŹĒæÕĘų²ĪÓė·“Ó¦£¬ŅŅČĻĪŖŹĒ°×Īķ²ĪÓė·“Ó¦”£
¢ŁĪ“Ö¤Źµø÷×ŌµÄ¹Ūµć£¬ŌŚŌŹµŃ黳“”ÉĻ£ŗ¼×ŌŚŌÓŠ²Ł×÷Ö®Ē°Ōö¼ÓŅ»²½²Ł×÷£¬øĆ²Ł×÷ŹĒ____£»ŅŅŌŚA”¢B¼äŌö¼ÓĻ“ĘųĘæD£¬DÖŠŹ¢·ÅµÄŹŌ¼ĮŹĒ______”£
¢Ś½ųŠŠŹµŃ飬BÖŠĻÖĻó£ŗ
¼× | “óĮæ°×É«³Įµķ |
ŅŅ | ÉŁĮæ°×É«³Įµķ |
¼ģŃé°×É«³Įµķ£¬·¢ĻÖ¾ł²»ČÜÓŚĻ”ŃĪĖį”£½įŗĻĄė×Ó·½³ĢŹ½½āŹĶŹµŃéĻÖĻóŅģĶ¬µÄŌŅņ£ŗ___”£
(5)ŗĻ²¢£Ø4£©ÖŠĮ½Ķ¬Ń§µÄ·½°ø½ųŠŠŹŌŃ锣BÖŠĪŽ³ĮµķÉś³É£¬¶ųCÖŠ²śÉś°×É«³Įµķ£¬ÓÉ“ĖµĆ³öµÄ½įĀŪŹĒ_____”£
”¾“š°ø”æ2H2SO4(ÅØ)£«Cu ![]() CuSO4£«2H2O£«2SO2”ü BaSO4 »¹Ō 2NO+O2=2NO2 ĶØN2Ņ»¶ĪŹ±¼ä£¬Åųż×°ÖƵÄæÕĘų ±„ŗĶµÄNaHSO3ČÜŅŗ ¼×ÖŠSO42££«Ba2£«=BaSO4”ż£¬ŅŅÖŠ2Ba2£«£«2SO2£«O2£«2H2O=2BaSO4£«4H£«£¬°×ĪķµÄĮæŅŖŌ¶¶ąÓŚ×°ÖĆÖŠŃõĘųµÄĮæ SO2ÓėæÉČÜŠŌ±µµÄĒæĖįŃĪ²»ÄÜ·“Ӧɜ³ÉBaSO3³Įµķ
CuSO4£«2H2O£«2SO2”ü BaSO4 »¹Ō 2NO+O2=2NO2 ĶØN2Ņ»¶ĪŹ±¼ä£¬Åųż×°ÖƵÄæÕĘų ±„ŗĶµÄNaHSO3ČÜŅŗ ¼×ÖŠSO42££«Ba2£«=BaSO4”ż£¬ŅŅÖŠ2Ba2£«£«2SO2£«O2£«2H2O=2BaSO4£«4H£«£¬°×ĪķµÄĮæŅŖŌ¶¶ąÓŚ×°ÖĆÖŠŃõĘųµÄĮæ SO2ÓėæÉČÜŠŌ±µµÄĒæĖįŃĪ²»ÄÜ·“Ӧɜ³ÉBaSO3³Įµķ
”¾½āĪö”æ
£Ø1£©ÓÉĻÖĻóæÉÖŖ£¬AÖŠ·¢ÉśCuÓėÅØĮņĖįµÄ·“Ó¦£¬Éś³ÉĮņĖįĶ”¢¶žŃõ»ÆĮņŗĶĖ®£»
£Ø2£©CÖŠ°×É«³ĮµķĪŖĮņĖį±µ£¬SŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ»
£Ø3£©CÖŠŅŗĆęÉĻ·½·¢ÉśNO±»Ńõ»ÆÉś³É¶žŃõ»ÆµŖµÄ·“Ó¦£»
£Ø4£©¢ŁBÖŠŃĒĮņĖį±µ±»æÕĘųÖŠµÄŃõĘųŃõ»Æ£»ĮņĖįĖįĪķÄÜÓėB”¢CÖŠ±µĄė×Ó·“Ó¦£»¢Ś°×É«³Įµķ¾ł²»ČÜÓŚŃĪĖį£¬Ōņ°×É«³ĮµķĪŖĮņĖį±µ£¬ŅŌ“Ė·ÖĪö·¢ÉśµÄ·“Ó¦£»
£Ø5£©SO2ÓėæÉČÜŠŌ±µµÄĒæĖįŃĪ²»ÄÜ·“Ó¦£¬SO2ÓėæÉČÜŠŌ±µµÄČõĖįŃĪÄÜ·“Ó¦”£
£Ø1£©AÖŠÓŠĶŗĶÅØĮņĖį·“Ӧɜ³ÉĮņĖįĶŗĶ¶žŃõ»ÆĮņŗĶĖ®£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCu + 2H2SO4(ÅØ)![]() CuSO4+SO2”ü+2H2O£¬¹Ź“š°øĪŖ£ŗCu + 2H2SO4(ÅØ)
CuSO4+SO2”ü+2H2O£¬¹Ź“š°øĪŖ£ŗCu + 2H2SO4(ÅØ)![]() CuSO4+SO2”ü+2H2O£»
CuSO4+SO2”ü+2H2O£»
£Ø2£©¶žŃõ»ÆĮņČÜÓŚĖ®ĪŖŃĒĮņĖį£¬ÓėĻõĖį±µ·“Ӧɜ³ÉĮņĖį±µ³Įµķ£¬ĖłŅŌ°×É«³ĮµķĪŖBaSO4£¬ĖµĆ÷¶žŃõ»ÆĮņÓŠ»¹ŌŠŌ£¬¹Ź“š°øĪŖ£ŗBaSO4£»
£Ø3£©ĻõĖįøł±»»¹ŌĪŖŅ»Ńõ»ÆµŖĘųĢ壬ÓėæÕĘųÖŠµÄŃõĘų½Ó“„·“Ӧɜ³É¶žŃõ»ÆµŖ£¬ŗģ×ŲÉ«ĘųĢ壬·½³ĢŹ½ĪŖ£ŗ2NO+O2=2NO2£¬¹Ź“š°øĪŖ£ŗ2NO+O2=2NO2£»
£Ø4£©¢ŁAÖŠ°×ĪķæÉÄÜŗ¬ÓŠSO3»ņH2SO4£¬ŅņBÖŠ°×É«³Įµķ²»ČÜÓŚĻ”ŃĪĖį£¬ĖµĆ÷øĆ°×É«³ĮµķĪŖBaSO4£¬¼×Ķ¬Ń§ĪŖÅųż×°ÖĆÄŚæÕĘų¶ŌŹµŃé½į¹ūµÄÓ°Ļģ£¬ŌŚCuÓėÅØĮņĖį·“Ó¦Ē°£¬æÉĻČĶØŅ»»į¶łN2£¬Åųż×°ÖĆÖŠµÄæÕĘų”£ŅŅĶ¬Ń§ĪŖ³żČ„°×Īķ»ņSO2ÖŠµÄSO3£¬æÉŌŚA”¢B¼äŌö¼ÓŅ»øöŹ¢·ÅÅØĮņĖį»ņ±„ŗĶNaHSO3ČÜŅŗµÄĻ“ĘųĘ棻¢ŚÓÉÓŚ¼×Ķ¬Ń§Ć»ÓŠÅųż°×ĪķµÄøÉČÅ£¬¹ŹÉś³ÉBaSO4³ĮµķµÄĄė×Ó·½³ĢŹ½ĪŖSO42£+Ba2£«=BaSO4”ż£»ŅŅĶ¬Ń§Ć»ÓŠÅųżæÕĘųµÄøÉČÅ£¬ĘäÉś³ÉBaSO4µÄĄė×Ó·½³ĢŹ½ĪŖ2Ba2£«+2SO2+O2+2H2O=2BaSO4”ż+4H£«£¬¹Ź“š°øĪŖ£ŗ¼×ÖŠSO42££«Ba2£«=BaSO4”ż£¬ŅŅÖŠ2Ba2£«£«2SO2£«O2£«2H2O=2BaSO4£«4H£«£¬°×ĪķµÄĮæŅŖŌ¶¶ąÓŚ×°ÖĆÖŠŃõĘųµÄĮ棻
£Ø5£©ŗĻ²¢¼×”¢ŅŅĮ½Ķ¬Ń§µÄ·½°ø½ųŠŠŹµŃ鏱£¬BÖŠĪŽ³ĮµķÉś³É£¬CÖŠ²śÉś°×É«³Įµķ£¬ĖµĆ÷SO2ÓėæÉČÜŠŌ±µµÄĒæĖįŃĪ²»ÄÜ·“Ӧɜ³ÉBaSO3³Įµķ£¬¹Ź“š°øĪŖ£ŗSO2ÓėæÉČÜŠŌ±µµÄĒæĖįŃĪ²»ÄÜ·“Ӧɜ³ÉBaSO3³Įµķ”£


 æŖŠÄæģĄÖ¼ŁĘŚ×÷ŅµŹī¼Ł×÷ŅµĪ÷°²³ö°ęÉēĻµĮŠ“š°ø
æŖŠÄæģĄÖ¼ŁĘŚ×÷ŅµŹī¼Ł×÷ŅµĪ÷°²³ö°ęÉēĻµĮŠ“š°ø ĆūĢāѵĮ·ĻµĮŠ“š°ø
ĆūĢāѵĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŌøõĢśæó[Ö÷ŅŖ³É·ÖĪŖFe(CrO2)2]£¬ŗ¬ÓŠAl2O3”¢Fe2O3”¢SiO2µČŌÓÖŹĪŖÖ÷ŅŖŌĮĻÉś²śÖŲøõĖįÄĘ¾§Ģå(Na2Cr2O7”¤2H2O)µÄÖ÷ŅŖ¹¤ŅÕĮ÷³ĢČēĻĀ£¬¹ŲÓŚøĆĮ÷³ĢĖµ·Ø“ķĪóµÄŹĒ£Ø £©

A.ģŃÉÕÉś³ÉNa2CrO4µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ4Fe(CrO2)2+8Na2CO3+7O2![]() 2Fe2O3+8Na2CrO4 +8CO2
2Fe2O3+8Na2CrO4 +8CO2
B.SiO2ŌŚ”°½ž³ö¹żĀĖ”±²½ÖčÖŠŗĶFe2O3Ņ»Ęš³żČ„
C.Na2CrO4µ½Na2Cr2O7×Ŗ»ÆµÄŌĄķĪŖ£ŗ2H£«+2CrO42£![]() Cr2O72£+H2O
Cr2O72£+H2O
D.øĆ¹¤ŅÕÖŠ”°ģŃÉÕ”±²śÉśµÄCO2æÉÓĆÓŚ”°³żŌÓ”±²½ÖčŅŌ½ŚŌ¼Éś²ś³É±¾£¬ĪŖĶźČ«³żČ„AlO2££¬·¢ÉśµÄĄė×Ó·“Ó¦ĪŖ£ŗCO2+AlO2£+2H2O=Al(OH)3”ż+HCO3£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµē»Æѧ·Ø»¹Ō¶žŃõ»ÆĢ¼£¬²»½öÄÜ»ŗ½āĪĀŹŅŠ§Ó¦»¹ÄܵƵ½ŅŅĻ©”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŅŃÖŖ£ŗC2H4(g)+H2O(g)=C2H5OH(g) ¦¤H1=-45.8kJ”¤mol-1
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) ¦¤H2=-1277.0kJ”¤mol-1
Ōņ2CO2(g)+2H2O(g)=C2H4(g)+3O2(g)¦¤H3=____”£
£Ø2£©µē»Æѧ·Ø»¹Ō¶žŃõ»ÆĢ¼ĪŖŅŅĻ©ŌĄķČēĶ¼ĖłŹ¾”£
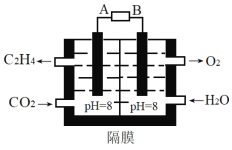
AĪŖµēŌ“µÄ___¼«(Ģī”°Õż”±»ņ”°øŗ”±)£¬Ņõ¼«µē¼«·“Ó¦Ź½ĪŖ___”£µēĀ·ÖŠ×ŖŅĘ0.2molµē×Ó£¬ĄķĀŪÉĻ²śÉśŃõĘų___L£Ø±ź×¼×“æö£©”£
£Ø3£©Ķ×÷Ņõ¼«ÄÜĢįøß»¹Ō²śĪļŅŅĻ©µÄŃ”ŌńŠŌ£¬Ė®ČÜŅŗÖŠ¶žŃõ»ÆĢ¼ŌŚĶ±ķĆę»¹ŌĪŖŅŅĻ©µÄ»śĄķČēĶ¼ĖłŹ¾£Ø²ĪÓė·“Ó¦µÄĖ®·Ö×Ó¼°ĘäĖüÉś³ÉĪ¢Į£Ī“»³ö£©”£ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ___£ØĢī±źŗÅ£©”£
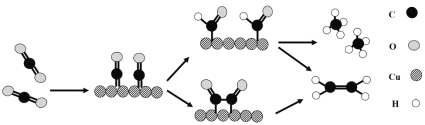
A.ĶŹĒ¶žŃõ»ÆĢ¼×Ŗ»ÆĪŖŅŅĻ©µÄ“߻ƼĮ
B.¶žŃõ»ÆĢ¼»¹Ō²śĪļÓŠ¼×ĶéŗĶŅŅĻ©
C.Į½øö·“Ó¦Ąś³Ģ¶¼ŹĒĻČ¼ÓĒāŌŁ³żŃõ
D.Į½øö·“Ó¦Ąś³Ģ¶¼³öĻÖĢ¼Ńõ¼üµÄ¶ĻĮŃÓėĢ¼Ģ¼¼üµÄŠĪ³É
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄūÓĆŗ¬Ģ¼»ÆŗĻĪļŗĻ³ÉČ¼ĮĻŹĒ½ā¾öÄÜŌ“Ī£»śµÄÖŲŅŖ·½·Ø£¬ŅŃÖŖCO(g)£«2H2(g)![]() CH3OH(g)·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»ÆĒéæöČēĶ¼ĖłŹ¾£¬ĒśĻߢńŗĶĒśĻߢņ·Ö±š±ķŹ¾²»Ź¹ÓĆ“ß»Æ¼ĮŗĶŹ¹ÓĆ“ß»Æ¼ĮµÄĮ½ÖÖĒéæö”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø £©
CH3OH(g)·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»ÆĒéæöČēĶ¼ĖłŹ¾£¬ĒśĻߢńŗĶĒśĻߢņ·Ö±š±ķŹ¾²»Ź¹ÓĆ“ß»Æ¼ĮŗĶŹ¹ÓĆ“ß»Æ¼ĮµÄĮ½ÖÖĒéæö”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø £©
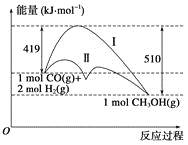
A.øĆ·“Ó¦µÄ¦¤H£½£«91 kJ”¤mol£1
B.¼ÓČė“߻ƼĮ£¬øĆ·“Ó¦µÄ¦¤H±äŠ”
C.·“Ó¦ĪļµÄ×ÜÄÜĮæ“óÓŚÉś³ÉĪļµÄ×ÜÄÜĮæ
D.Čē¹ūøĆ·“Ӧɜ³ÉŅŗĢ¬CH3OH£¬Ōņ¦¤HŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼īŹ½ĀČ»ÆĶŹĒÖŲŅŖµÄĪŽ»śÉ±¾ś¼Į”£
(1)¼īŹ½ĀČ»ÆĶÓŠ¶ąÖÖÖʱø·½·Ø
¢Ł·½·Ø1£ŗ45 ~ 50”ꏱ£¬ĻņCuClŠü×ĒŅŗÖŠ³ÖŠųĶØČėæÕĘųµĆµ½Cu2 (OH)2 Cl2”¤3H2O£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____________”£
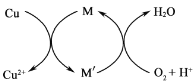
¢Ś·½·Ø2£ŗĻČÖʵĆCuCl2£¬ŌŁÓėŹÆ»ŅČ鷓Ӧɜ³É¼īŹ½ĀČ»ÆĶ”£CuÓėĻ”ŃĪĖįŌŚ³ÖŠųĶØČėæÕĘųµÄĢõ¼žĻĀ·“Ӧɜ³ÉCuCl2£¬Fe3+¶ŌøĆ·“Ó¦ÓŠ“ß»Æ×÷ÓĆ,Ęä“ß»ÆŌĄķČēĶ¼ĖłŹ¾”£M'µÄ»ÆѧŹ½ĪŖ______”£
(2)¼īŹ½ĀČ»ÆĶÓŠ¶ąÖÖ×é³É£¬æɱķŹ¾ĪŖCua(OH)bClc”¤xH2O”£ĪŖ²ā¶Øij¼īŹ½ĀČ»ÆĶµÄ×é³É£¬½ųŠŠĻĀĮŠŹµŃé£ŗ
¢Ł³ĘȔѳʷ2.2320g£¬ÓĆÉŁĮæĻ”HNO3ČܽāŗóÅä³É100.00mLČÜŅŗA£»
¢ŚČ”25. 00mLČÜŅŗA£¬¼ÓČė×ćĮæAgNO3ČÜŅŗ£¬µĆAgCl 0. 3444g£»
¢ŪĮķČ”25. 00mLČÜŅŗA£¬µ÷½ŚpH 4 ~ 5£¬ÓĆÅضČĪŖ0.08000mol”¤L-1µÄEDTA(Na2H2Y”¤2H2O)±ź×¼ČÜŅŗµĪ¶ØCu2+ (Ąė×Ó·½³ĢŹ½ĪŖCu2++ H2Y2£=CuY2£+2H+)£¬µĪ¶ØÖĮÖÕµć£¬Ļūŗıź×¼ČÜŅŗ60.00mL”£Ķعż¼ĘĖćČ·¶ØøĆѳʷµÄ»ÆѧŹ½(Š“³ö¼ĘĖć¹ż³Ģ)”£_____________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĻĀĮŠŹµŃé²Ł×÷ŗĶĻÖĻóĖłµĆµ½µÄ½įĀŪÕżČ·µÄŹĒ
Ń”Ļī | ŹµŃé²Ł×÷ŗĶĻÖĻó | ½įĀŪ |
A | ŹŅĪĀĻĀ£¬Ļņ±½·ÓÄĘČÜŅŗÖŠĶØČė×ćĮæCO2£¬ČÜŅŗ±ä»ė×Ē”£ | Ģ¼ĖįµÄĖįŠŌ±Č±½·ÓµÄĒæ |
B | ŹŅĪĀĻĀ£¬ĻņÅØ¶Č¾łĪŖ0.1 mol”¤LØC1µÄBaCl2ŗĶCaCl2»ģŗĻČÜŅŗÖŠµĪ¼ÓNa2SO4ČÜŅŗ£¬³öĻÖ°×É«³Įµķ”£ | Ksp£ØBaSO4£©£¼Ksp£ØCaSO4£© |
C | ŹŅĪĀĻĀ£¬ĻņFeCl3ČÜŅŗÖŠµĪ¼ÓÉŁĮæKIČÜŅŗ£¬ŌŁµĪ¼Ó¼øµĪµķ·ŪČÜŅŗ£¬ČÜŅŗ±äĄ¶É«”£ | Fe3+µÄŃõ»ÆŠŌ±ČI2µÄĒæ |
D | ŹŅĪĀĻĀ£¬ÓĆpHŹŌÖ½²āµĆ£ŗ0.1mol”¤LØC1Na2SO3ČÜŅŗµÄpHŌ¼ĪŖ10£»0.1mol”¤LØC1NaHSO3ČÜŅŗµÄpHŌ¼ĪŖ5”£ | HSO3ØC½įŗĻH£«µÄÄÜĮ¦±Č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½³ĢŹ½ÖŠ£¬ÕżČ·µÄŹĒ
A.ÓƶčŠŌµē¼«µē½āMgCl2ČÜŅŗ£ŗ2Cl-+H2O![]() 2OH-+Cl2”ü+H2”ü
2OH-+Cl2ӟ+H2ӟ
B.Ģ¼ĖįÄĘČÜŅŗĻŌ¼īŠŌ£ŗCO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
C.ĀČĘųĶØČėĄäĖ®ÖŠ£ŗCl2 £«H2O ![]() Cl££«ClO££«2H+
Cl££«ClO££«2H+
D.Ģ¼ĖįĆ¾Šü×ĒŅŗÖŠ¼Ó“×Ėį£ŗCO32££«2CH3COOH£½ 2CH3COO££«CO2”ü£«H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒāĘųŹĒŅ»ÖÖĒå½ąÄÜŌ“£¬ĒāĘųµÄÖĘČ”Óė“¢“ęŹĒĒāÄÜŌ“ĄūÓĆĮģÓņµÄŃŠ¾æČČµć”£
(1)ČČ·Ö½ā·ØÖĘĒā”£Ä³ĪĀ¶Č£¬H2O(g) ![]() H2(g)+1/2O2(g)”£øĆ·“Ó¦Ę½ŗā³£Źż±ķ“ļŹ½K=_____
H2(g)+1/2O2(g)”£øĆ·“Ó¦Ę½ŗā³£Źż±ķ“ļŹ½K=_____
(2)ČČ»Æѧѻ·ÖĘĒā”£ÖʱøH2µÄ·“Ó¦²½ÖčČēĻĀ£ŗ
¢ŁBr2(g) + CaO(s) = CaBr2(s) + 1/2O2(g) ¦¤H=£73 kJ”¤mol-1
¢Ś3FeBr2(s) + 4H2O(g) = Fe3O4(s) + 6HBr(g) + H2(g) ¦¤H=+384 kJ”¤mol-1
¢ŪCaBr2(s) + H2O (g) = CaO(s) + 2HBr(g) ¦¤H=+212 kJ”¤mol-1
¢ÜFe3O4(s)+8 HBr(g) = Br2(g) + 3FeBr2(s) + 4H2O(g) ¦¤H=£274 kJ”¤mol-1
Ōņ H2O(g) ![]() H2(g)+1/2O2(g) ¦¤H =_________kJ”¤mol£1”£
H2(g)+1/2O2(g) ¦¤H =_________kJ”¤mol£1”£
(3)¹āµē»Æѧ·Ö½āÖĘĒā£¬īŃĖįļČ¹āµē¼«:4OH-£4e- ![]() O2+2H2O£¬Ōņ²¬µē¼«µÄµē¼«·“Ó¦ĪŖ_______”£
O2+2H2O£¬Ōņ²¬µē¼«µÄµē¼«·“Ó¦ĪŖ_______”£
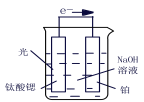
(4)Ė®ĆŗĘų·ØÖĘĒā”£CO(g) + H2O(g) ![]() CO2(g)+ H2(g) ¦¤H <0£¬ŌŚ850”ꏱ£¬K=1”£
CO2(g)+ H2(g) ¦¤H <0£¬ŌŚ850”ꏱ£¬K=1”£
¢Ł ČōÉżøßĪĀ¶Čµ½950”ꏱ£¬“ļµ½Ę½ŗāŹ±K_________1(Ģī”°£¾”±”¢”°£¼”±»ņ ”°£½”±)”£
¢Ś 850”ꏱ£¬ČōĻņŅ»ČŻ»żæɱäµÄĆܱÕČŻĘ÷ÖŠĶ¬Ź±³äČė1.0 mol CO”¢3.0 mol H2O”¢1.0 mol CO2 ŗĶx mol H2£¬ČōŅŖŹ¹ÉĻŹö·“Ó¦æŖŹ¼Ź±ĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬ŌņxÓ¦Āś×ćµÄĢõ¼žŹĒ_________”£
(5)¼×ĶéÖĘĒā”£½«1.0 mol CH4ŗĶ2.0 mol H2O (g)ĶØČėČŻ»żĪŖ100 LµÄ·“Ó¦ŹŅ£¬ŌŚŅ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗCH4(g) + H2O (g)£½CO (g) + 3H2(g)”£²āµĆ“ļµ½Ę½ŗāĖłŠčµÄŹ±¼äĪŖ5 min£¬CH4µÄĘ½ŗā×Ŗ»ÆĀŹĪŖ50%£¬ŌņÓĆH2±ķŹ¾øĆ·“Ó¦µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ_____”£
(6)LiBH4¾ßÓŠ·Ē³£øߵē¢ĒāÄÜĮ¦£¬·Ö½āŹ±Éś³ÉĒā»Æļ®ŗĶĮ½ÖÖ·Ē½šŹōµ„ÖŹ”£øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄÜÕżČ·±ķŹ¾ĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½µÄŹĒ(””””)
A.Ļņ³ĪĒåŹÆ»ŅĖ®ÖŠĶØČėÉŁĮæSO2ĘųĢå£ŗCa2£«£«SO2=CaSO3”ż
B.¹żĮæSO2ĘųĢåĶØČėĒāŃõ»ÆÄĘČÜŅŗÖŠ£ŗSO2£«OH£=![]()
C.SO2ĘųĢåĶØČėäåĖ®ÖŠ£ŗSO2£«Br2£«H2O=2H£«£«2Br££«![]()
D.ĻņĒāĮņĖįÖŠĶØČėĀČĘų£ŗS2££«Cl2=S”ż£«2Cl£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com