
|
将0.02 mol铜片溶于100 mL 9 mol/L HNO3中,产生336 mL气体(只含NO、NO2).该气体与一定量O2混合后,用一定量NaOH溶液完全吸收并恰好全部生成盐,则通入的O2体积可能为(气体体积均为标准状况) | |
A. |
11.2 mL |
B. |
22.4 mL |
C. |
56.2 mL |
D. |
67.2 mL |
科目:高中化学 来源: 题型:阅读理解
 2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是
2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是查看答案和解析>>
科目:高中化学 来源:江西省白鹭洲中学2010-2011学年高二下学期第三次月考化学试题 题型:013
|
将1.92 g Cu放入含0.02 mol HNO3的稀硝酸中,要使铜完全溶解,理论上要加入2 mol/L的稀硫酸溶液的体积为 | |
| [ ] | |
A. |
10 mL |
B. |
15 mL |
C. |
20 mL |
D. |
25 mL |
查看答案和解析>>
科目:高中化学 来源:上海市杨浦区2011届高三一模化学试题 题型:038
科研人员发现,一些化学反应在固体之间发生和在水溶液中发生,产物不同.
铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+1、+2.
将CuCl2·2H2O晶体和NaOH固体混合研磨,生成物中有一黑色的固体A.A不溶于水,但可溶于稀硫酸生成蓝色溶液B.
(1)A的化学式为________;A不同于CuCl2和NaOH在溶液中反应所得产物的可能原因是________.
(2)在含0.02 mol B的溶液中加入适量氨水恰好完全反应,得到浅蓝色沉淀C和无色的溶液D;C溶于盐酸后,加入足量的BaCl2溶液,生成2.33 g白色沉淀;无色的溶液D中加入足量的NaOH,加热收集到无色有刺激性气味的气体E.
①通过计算确定C的化学式.
②E是________(填物质名称),E在标准状况下的体积为________mL.
(3)若向B中加过量氨水后,再通入SO2至微酸性,最终得到白色沉淀F和无色的溶液.分析知,F是不含结晶水的复盐,其部分元素的质量分数为:Cu 39.31%、S 19.84%、N 8.67%.
①通过计算确定F的化学式.
②写出由B生成F的化学方程式.
(4)将F与中等浓度的硫酸混合加热,会放出无色有刺激性气味的气体,析出紫红色沉淀,同时得到蓝色的溶液.写出该反应的化学方程式.
查看答案和解析>>
科目:高中化学 来源: 题型:
分别回答下列问题。(10分)
(1)从H+、Na+、Cu2+、Cl-、![]() 中选出两种离子组成电解质,按下列要求进行电解(使用惰性电极),将电解质的化学式填空:(只写出一种即可)
中选出两种离子组成电解质,按下列要求进行电解(使用惰性电极),将电解质的化学式填空:(只写出一种即可)
①电解过程中溶液颜色变浅且水量不变_______________________;
②电解过程中电解质含量不变,水量减少_______________________;
③电解过程中,两极析出气体的体积比为1∶1__________。
(2)①用惰性电极电解硫酸铜溶液,若阴极上有1.6克铜析出,则阳极上产生的气体
在标准状况下的体积约为 ;
②用铂电极电解0.02 mol/L硫酸铜溶液,直至铜完全析出,所得溶液中氢离子浓度为
(忽略溶液体积的变化) ;
③已知下列两个热化学方程式2H2(g)+O2(g)=2H2O(1) △H= -571.6KJ
 C3H8(g) +5O2(g)=3CO2(g)+4H2O(1) △H=-2220.0kJ
C3H8(g) +5O2(g)=3CO2(g)+4H2O(1) △H=-2220.0kJ
实验测得,5mol氢气和丙烷的混合气体完全燃烧时放热
3847kJ,则混合气体中氢气与丙烷的体积比是 。
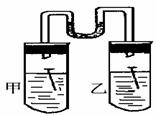
(3)如右图所示,甲、乙两试管中各放一枚铁钉,甲试管中
为NaCl溶液,乙试管为稀醋酸溶液,数天后观察到的现象
是 ,甲中正极反应为
,负极反应式为,乙中正极反应为 ,负极反应式为 。
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com