
【题目】用NA表示阿伏加德罗常数的值。下列叙述正确的有
①3lg白磷中含有1.5NA个P-P键
②1L0.1mol·L-1的Na2CO3溶液中所含阴离子的总数目为0.1NA
③标准状况下,22.4LHF 中含有NA个分子
④电解精炼铜时,若转移NA个电子,则阳极溶解32g铜
⑤将2.24L(标准状况)Cl2溶于水,转移的电子数为0.1NA
⑥常温下,含有0.2molH2SO4的浓硫酸与足量铜反应,生成SO2分子的数目小于0.1NA
⑦142gNa2SO4 和Na2HPO4的固体混合物中所含阴、阳离子的总数目为3NA
⑧NA个Fe(OH)3胶体粒子的质量为107g
A.2项B.3项C.4项D.5项
【答案】B
【解析】
①3lg白磷中含有P—P键数目![]() ,故①正确;②1L0.1 molL1的Na2CO3溶液中碳酸钠物质的量n =0.1 molL1×1L=0.1mol,碳酸根水解生成碳酸氢根和氢氧根,因此0.1mol碳酸钠溶液中含阴离子的总数目大于0.1NA,故②错误;③标准状况下,HF是液体,因此无法计算分子数目,故③错误;④电解精炼铜时,阳极是粗铜,先锌失去电子,再是铁失去电子,再是铜失去电子,因此转移NA个电子,则阳极溶解铜小于32g,故④错误;⑤将2.24L(标准状况)Cl2物质的量为1mol,氯气溶于水是可逆反应,因此转移的电子数小于0.1NA,故⑤错误;⑥常温下,含有0.2mol H2SO4的浓硫酸与足量铜反应不反应,因此生成SO2分子的数目小于0.1NA,故⑥正确;⑦Na2SO4和Na2HPO4的摩尔质量都为142 gmol1,且两种物质都含有3mol离子,因此142gNa2SO4和Na2HPO4的固体混合物物质的量为1mol,所含阴、阳离子的总数目为3NA,故⑦正确;⑧氢氧化铁胶体粒子是氢氧化铁的集合体,NA个Fe(OH)3胶体粒子的质量为大于107g,故⑧错误;因此①⑥⑦正确;故B正确。
,故①正确;②1L0.1 molL1的Na2CO3溶液中碳酸钠物质的量n =0.1 molL1×1L=0.1mol,碳酸根水解生成碳酸氢根和氢氧根,因此0.1mol碳酸钠溶液中含阴离子的总数目大于0.1NA,故②错误;③标准状况下,HF是液体,因此无法计算分子数目,故③错误;④电解精炼铜时,阳极是粗铜,先锌失去电子,再是铁失去电子,再是铜失去电子,因此转移NA个电子,则阳极溶解铜小于32g,故④错误;⑤将2.24L(标准状况)Cl2物质的量为1mol,氯气溶于水是可逆反应,因此转移的电子数小于0.1NA,故⑤错误;⑥常温下,含有0.2mol H2SO4的浓硫酸与足量铜反应不反应,因此生成SO2分子的数目小于0.1NA,故⑥正确;⑦Na2SO4和Na2HPO4的摩尔质量都为142 gmol1,且两种物质都含有3mol离子,因此142gNa2SO4和Na2HPO4的固体混合物物质的量为1mol,所含阴、阳离子的总数目为3NA,故⑦正确;⑧氢氧化铁胶体粒子是氢氧化铁的集合体,NA个Fe(OH)3胶体粒子的质量为大于107g,故⑧错误;因此①⑥⑦正确;故B正确。
综上所述,答案为B。


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】下列说法或有关化学用语的表达正确的是( )
A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量
B.基态Fe原子的价电子轨道表示式为
C.因硫元素电负性比磷元素大,故硫元素第一电离能比磷元素第一电离能大
D.根据原子核外电子排布的特点,Cu在元素周期表中位于s区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置中,有如下实验现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面。以下有关解释不合理的是
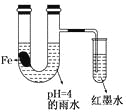
A. 生铁片中所含的碳能增强铁的抗腐蚀性
B. 雨水酸性较强,生铁片开始发生析氢腐蚀
C. 导管内墨水液面回升时,正极反应式:O2+2H2O+4e—==4OH-
D. 随着反应的进行,U型管中雨水的酸性逐渐减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度、相同容积的四个密闭容器中进行同样的可逆反应:2X(g)+Y(g)![]() 3W(g)+2Z(g) △H=﹣Q KJ/mol,起始时充入气体的物质的量及平衡时体系能量变化数据如表,下列说法正确的是( )
3W(g)+2Z(g) △H=﹣Q KJ/mol,起始时充入气体的物质的量及平衡时体系能量变化数据如表,下列说法正确的是( )
X | Y | W | Z | 反应体系能量变化 | |
甲 | 2mol | 1mol | 放出a kJ/mol | ||
乙 | 1mol | 1mol | 放出b kJ/mol | ||
丙 | 2mol | 2mol | 放出c kJ/mol | ||
丁 | 3mol | 2mol | 吸收d kJ/mol |
A.X的转化率为:甲<乙<丙
B.c+d<Q
C.平衡时,甲容器中的反应速率比丁容器中的慢
D.平衡时丙容器中Z的物质的量浓度最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是A~G七种元素的电子排布:
元素 电子排布 电子层 | A | B | C | D | E | F | G |
K | 1 | 2 | 2 | 2 | 2 | 2 | 2 |
L | 4 | 5 | 6 | 8 | 8 | 8 | |
M | 1 | 3 | 7 |
试根据由上述元素构成的物质的化学式回答下列问题。
(1)写出一种常见的由非极性键形成的双原子分子:____________________。
(2)写出一种由极性键形成的双原子分子:____________________。
(3)写出一种由极性键形成的三原子分子:____________________。
(4)写出一种由三种元素形成的既含离子键又含共价键的化合物:__________,其电子式为____________________。
(5)写出一种既含离子键又含非极性键的化合物:__________,其电子式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸阿比朵尔,适合治疗由 A、B 型流感病毒引起的上呼吸道感染,2020 年入选新冠肺炎试用药物,其合成路线:
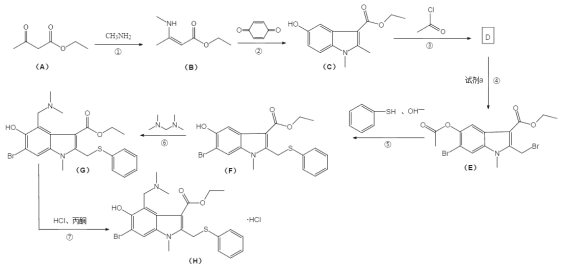
回答下列问题:
(1)有机物 A 中的官能团名称是______________和______________。
(2)反应③的化学方程式______________。
(3)反应④所需的试剂是______________。
(4)反应⑤和⑥的反应类型分别是______________、______________。
(5)I 是 B 的同分异构体,具有两性并能与碳酸氢钠溶液反应放出气体,写出具有六元 环结构的有机物 H 的结构简式______________。 (不考虑立体异构,只需写出 3 个)
(6)已知:两分子酯在碱的作用下失去一分子醇生成β—羟基酯的反应称为酯缩合反应,也称为 Claisen (克莱森)缩合反应,如: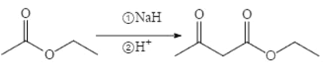 ,设计由乙醇和
,设计由乙醇和![]() 制备
制备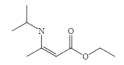 的合成线路______________。(无机试剂任选)
的合成线路______________。(无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家认为,氢气是21世纪一种高效而无污染的理想能源。
(1)为了有效发展氢能源,首先必须制得廉价的氢气,下列可供开发较经济且资源可持续利用的制氢气的方法是___。
A.电解水 B.锌和稀硫酸反应 C.催化光解海水 D.分解天然气
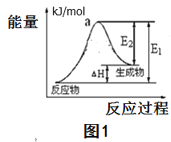
(2)用水分解获得氢气的能量变化如图1所示,则此反应的焓变△H=___kJ/mol。(请用关于E1,E2的代数式表示)。
(3)以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+H2O(g)═CO(g)+3H2(g) △H=+206.2kJmol﹣1
CH4(g)+CO2(g)═2CO(g)+2H2(g) △H=+247.4kJmol﹣1
则CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=___kJmol﹣1
(4)某固体酸膜氢氧燃料电池以Ca(HSO4)2固体为电解质传递H+,其基本结构如图2所示,请按要求回答下列问题:
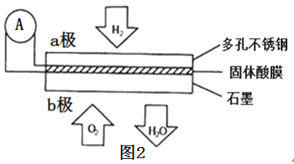
①b极上的电极反应式为___。
②此电池工作时每消耗4.48L(标准状况下)H2,转移电子___mol。
③若将这些电子用于铅蓄电池(两极板上分别覆盖有Pb、PbO2,电解质溶液是H2SO4溶液)充电,铅蓄电池中产生H2SO4的物质的量为___mol,铅蓄电池阳极发生的反应为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图涉及到的物质所含元素中,除一种元素外,其余均为1~18号元素。
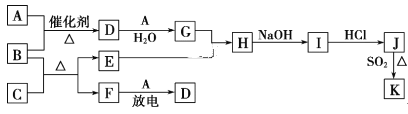
已知:A、F为无色气体单质,B为具有刺激性气味的气体,C为黑色氧化物,E为红色金属单质(部分反应的产物未列出)。请回答下列问题:
(1)D的化学式为__;F的结构式为__。
(2)A与B生成D的反应在工业上是生产__的反应原理之一。
(3)E与G的稀溶液反应的离子方程式为__。
(4)B和C反应的化学方程式为__。
(5)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式:__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com