
| A. | 加热 | B. | 保持容器体积不变,增加H2输入量 | ||
| C. | 充入N2,保持容器内压强不变 | D. | 充入N2,保持容器体积不变 |
分析 对于反应Fe2O3+3H2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O来说,升高温度、增大浓度或压强、增大固体表面积可增大反应速率,以此解答该题.
解答 解:A.加热反应速率加快,故A不选;
B.保持容器体积不变,增加H2的输入量,氢气的浓度增大,反应速率增大,故B不选;
C.充入N2,保持容器内压强不变,则体积应增大,但对于反应气体来说,浓度减小,则反应速率减小,故C不选;
D.充入N2,保持容器内体积不变,反应气体的浓度不变,则反应速率不变,故D选.
故选D.
点评 本题考查化学反应速率的影响因素,为高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大,易错点为C、D,注意压强与浓度的关系.


科目:高中化学 来源: 题型:选择题
| A. | ClO2 | B. | NaClO4 | C. | HClO | D. | NaClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在强酸性条件下Na+、IO-、K+、可以大量共存 | |
| B. | 在强碱性条件下K+、AlO2-、Na+、NO3-可以大量共存 | |
| C. | 在水溶液中H+、NH4+、SiO32-、Cl-不能大量共存 | |
| D. | 在强酸性条件下NH4+、K+、SO32-、S2-可以大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量数是60 | B. | 质子数是27 | C. | 中子数是33 | D. | 电子数是33 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
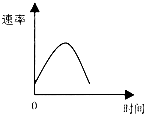 把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由下图表示.在下列因素中对产生H2速率有影响的是( )
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由下图表示.在下列因素中对产生H2速率有影响的是( )| A. | ①④ | B. | ③④ | C. | ①②③ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn+CuSO4═ZnSO4+Cu | B. | 2HI+Cl2═I2+2HCl | ||
| C. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | D. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 操作及现象 |
| i | 取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色 |
| ii | 向i所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液,产生无色气体(经检验为O2),溶液变为深红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 使用漏斗、滤纸、玻璃棒等进行过滤实验 | |
| B. | 用带玻璃塞的试剂瓶盛盐酸 | |
| C. | 在表面皿蒸发浓缩NaCl溶液 | |
| D. | 配制100mL浓度为0.10 mol•L-1Na Cl溶液时,在容量瓶中溶解、定容 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(X2)=0.15mol/L | B. | c(Y2)=0.9mol/L | C. | c(Z2)=0.3mol/L | D. | c(Q2)=0.5mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com