
某同学利用下图装置,用0.1000mol/L的氢氧化钾溶液测定某未知浓度的盐酸溶液的物质的量浓度,,其操作可分解为如下几步:
A.用标准溶液润洗滴定管2~3次
B.取标准KOH溶液注入碱式滴定管至刻度0以上2~3cm
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.调节液面至0或0以下刻度,记下读数
E. 移取20.00mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞
F. 把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,并记下滴定管液面的刻度读数。
G.把锥形瓶里的溶液倒掉,用蒸馏水把锥形瓶洗涤干净。按上述操作重复一次,并记下滴定前后液面刻度的读数。
就此实验完成填空:
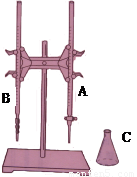
(1)上图所示是 常用的仪器,(填实验名称)。图中A是 (填仪器名称)
(2)判断到达滴定终点的实验现象是:___ ____
(3)上述E步骤操作之前,先用蒸馏水润洗锥形瓶,则对滴定结果的影响是
(填“偏高”、 “ 偏低”或“无影响”)。
(4)重复做该实验4次。所得实验数据如下表:
|
实验次数 |
c(KOH)/mol·L-1 |
B中起点刻度 |
B中终点刻度 |
V(HCl)/ml |
|
1 |
0.1000 |
0 |
24.95 |
25.00 |
|
2 |
0.1000 |
0 |
24.96 |
25.00 |
|
3 |
0.1000 |
0 |
24.50 |
25.00 |
|
4 |
0.1000 |
0 |
24.94 |
25.00 |
请你确定盐酸的物质的量浓度为 mol/L
(1)酸碱中和滴定(2分) 酸式滴定管(2分)
(2)溶液由无色变为红色并在半分钟内不褪色(2分)
(3)无影响 (2分) (4) 0.09980 mol/L(2分)
【解析】
试题分析:(2)滴定时,当溶液颜色变化且半分钟内不变色,可说明达到滴定终点,故答案为:无色变浅红色且半分钟内不褪色;
(3)锥形瓶中的蒸馏水在滴定过程中对物质的浓度没有影响。
(5)取1、2、4体积进行计算,所用标准液的平均体积为(24.95+24.96+24.94)mL/3="24.95" mL,则c(酸)= 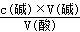 =0.09980mol/L,
=0.09980mol/L,
故答案为:0.09980。
考点:中和滴定
点评:本题考查酸碱中和滴定实验,题目难度不大,注意把握实验的原理、步骤、方法以及注意事项,把握实验基本操作。


科目:高中化学 来源:学习周报 化学 人教课标高一版(必修1) 2009-2010学年 第16期 总第172期 人教课标版 题型:058
某同学利用下图装置完成如下实验:在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后溶液恢复为无色.则此溶液可能是
________,加热时溶液由无色变为红色的原因是___________.查看答案和解析>>
科目:高中化学 来源:2012-2013学年陕西省三原县北城中学高二上学期期中考试化学试卷(带解析) 题型:实验题
某同学利用下图装置,用0.1000mol/L的氢氧化钾溶液测定某未知浓度的盐酸溶液的物质的量浓度,,其操作可分解为如下几步:
| A.用标准溶液润洗滴定管2~3次 |
| B.取标准KOH溶液注入碱式滴定管至刻度0以上2~3cm |
| C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液 |
| D.调节液面至0或0以下刻度,记下读数 |
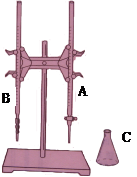
| 实验次数 | c(KOH)/mol·L-1 | B中起点刻度 | B中终点刻度 | V(HCl)/ml |
| 1 | 0.1000 | 0 | 24.95 | 25.00 |
| 2 | 0.1000 | 0 | 24.96 | 25.00 |
| 3 | 0.1000 | 0 | 24.50 | 25.00 |
| 4 | 0.1000 | 0 | 24.94 | 25.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(16分)X、Y、Z是不同短周期的三种元素,原子序数依次增大,Z是金属元素;A、B化合物均只含其中两种元素,一定条件下,A和水缓慢作用生成化合物M和无色刺激性气体B,B为三角锥形分子,单质Z和化合物M 均既可与盐酸反应,又可与NaOH溶液反应。回答下列问题:
(1)Z原子的电子排布式为 ;X、Y、Z三种元素的电负性由小到大的顺序是 (用元素符号表示)。
(2)A的化学式是 ;
(3)Z的盐酸盐溶液与过量NaOH溶液反应的离子方程式为 。
(4)800℃时,1.7gB被完全催化氧化放出QkJ热量,该反应的热化学方程式为 。
(5)某同学利用下图装置做电化学实验。请写出电极反应式:
Z单质表面: ,b极: 。

查看答案和解析>>
科目:高中化学 来源:安徽省巢湖市2010届高三第二次教学质量检测(理综化学)word版(含答案) 题型:填空题
(16分)X、Y、Z是不同短周期的三种元素,原子序数依次增大,Z是金属元素;A、B化合物均只含其中两种元素,一定条件下,A和水缓慢作用生成化合物M和无色刺激性气体B,B为三角锥形分子,单质Z和化合物M 均既可与盐酸反应,又可与NaOH溶液反应。回答下列问题:
(1)Z原子的电子排布式为 ;X、Y、Z三种元素的电负性由小到大的顺序是 (用元素符号表示)。
(2)A的化学式是 ;
(3)Z的盐酸盐溶液与过量NaOH溶液反应的离子方程式为 。
(4)800℃时,1.7gB被完全催化氧化放出QkJ热量,该反应的热化学方程式为 。
(5)某同学利用下图装置做电化学实验。请写出电极反应式:
Z单质表面: ,b极: 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com