
【题目】(1)在一定条件,可逆反应:mA+nB![]() pC达到平衡状态。
pC达到平衡状态。
①若A、C是气体,而且m+n=p,减小压强可使平衡发生移动,则平衡向____________(填“正”或“逆”)反应方向移动。
②若A、B、C均为气体,且m+n<p,加热后,可使混合气体平均摩尔质量增加,则正反应是____________(填“吸热”或“放热”)反应。
③若在反应过程中,C的物质的量n(C)随时间的变化关系如图所示(从t1时间开始对反应体系升高温度)。则a、b两点的正反应速率:v(a)____________v(b)(填“>”、“<”或“=”);

(2)Na2CO3溶液呈碱性,其原因是(用离子方程式表示)___________________;由同浓度的Na2CO3和NaHCO3组成的混合溶液中离子浓度由大到小的顺序为____________________;
(3)某温度下,纯水的c(H+)=3×10-7mol/L,Na2S和NaOH两溶液的pH均为12,则两溶液中由水电离出的c(H+)的比值为_________________;
【答案】
(1)①正;②放热;③<;
(2)CO32-+H2O![]() HCO3-+OH-;c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
HCO3-+OH-;c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
(3)9×1010或9×1010:1;
【解析】
试题分析:(1)①因增大压强,平衡向气体体积减小的方向移动,A、C是气体,而且m+n=p,所以B不是气体,则m<p,即平衡移动的方向是逆反应方向,故答案为:逆;
②若A、B、C均为气体,且m+n<p,加热后,可使混合气体平均摩尔质量增加,即平衡逆向移动,所以该反应的正反应为放热反应,故答案为:放热;
③a点温度小于b点温度,温度升高,反应速率增大,故答案为:<;
(2)Na2CO3是强碱弱酸盐,CO32-水解导致溶液呈碱性,水解离子方程式为CO32-+H2O![]() HCO3-+OH-;相同浓度的Na2CO3和NaHCO3组成的混合溶液中,HCO3-水解程度小于CO32-,则c(HCO3-)>c(CO32-),钠离子不水解,但其水解程度都较小,所以离子浓度大小顺序是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),故答案为:CO32-+H2O
HCO3-+OH-;相同浓度的Na2CO3和NaHCO3组成的混合溶液中,HCO3-水解程度小于CO32-,则c(HCO3-)>c(CO32-),钠离子不水解,但其水解程度都较小,所以离子浓度大小顺序是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),故答案为:CO32-+H2O![]() HCO3-+OH-;c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
HCO3-+OH-;c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
(3)在测得pH都等于12的NaOH溶液和Na2S溶液中,NaOH溶液由水电离的OH-浓度为=10-12mol/L,Na2S溶液由水电离的OH-浓度为=![]() =9×10-2mol/L,故两者比值为9×10-2:10-12mol=9×1010。
=9×10-2mol/L,故两者比值为9×10-2:10-12mol=9×1010。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】1mol过氧化钠与1.6mol碳酸氢钠固体混合后,在密闭的容器中加热充分反应,排出气体物质后冷却,残留的固体物质是 ( )
A. Na2CO3 B. NaOH、Na2CO3 C. Na2O2、 Na2CO3 D. Na2O2、 NaOH 、Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质各自形成的晶体,均属于分子晶体的化合物是( )
A.NH3 , H2 , CH4
B.PCl5 , CO2 , H2SO4
C.SO2 , SiO2 , P2O5
D.CCl4 , Na2S,H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的性质比较,正确的是( )
A.非金属性:P>S>Cl
B.碱性:NaOH>KOH>RbOH
C.气态氢化物稳定性:HF>HCl>HBr
D.酸性:H2SO4>HClO4>HBrO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 A(g)+3B(g)=2C(g)+2D(g)在四种不同情况下的反应速率分别为
①v(A)=0.45mol·L-1·min-1
②v(B)=0.6mol·L-1·s-1
③v(C)=0.4mol·L-1·s-1
④v(D)=0.45mol·L-1·s-1
下列有关反应速率的比较中正确的是
A. ④>③=②>① B. ④<③=②<① C. ①>②>③>④ D. ④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:
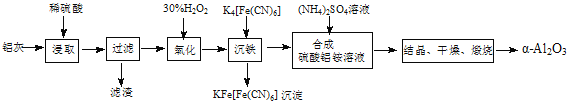
(1)铝灰中氧化铝与硫酸反应的化学方程式为 。
(2)图中“滤渣”的主要成分为 (填化学式)。
(3)加30%的H2O2溶液发生的离子反应方程式为 。
(4)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]![]() 2Al2O3 + 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
2Al2O3 + 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
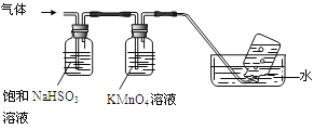
①集气瓶中收集到的气体是 (填化学式)。
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有 (填化学式)。
③KMnO4溶液褪色(MnO4-还原为Mn2+),发生的离子反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅丹(Pb3O4)可用于制作防锈涂料。该化合物中O的化合价为-2,Pb呈现两种化合价,一种为+4,则另一种为
A. -1 B. +1
C. +2 D. +3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH 溶液在如图所示的装置中进行中和反应。通过测定反应过程中 所放出的热量可计算中和热。回答下列问题:

①从实验装置上看,图中尚缺少的一种玻璃用品是__________________。
②实验中改用60 mL 0.50 mol/L盐酸跟50 mL 0.55 mol/L NaOH 溶液进行反应,与上述实验相比,所求的中和热_________(填“相等”或“不相等”)。
(2)①如图Ⅰ 表示10 mL量筒中液面的位置。A与B,B与C刻度间相差1 mL,如果刻度A为6,量筒中液体的体积是________mL。

②图Ⅱ表示50 mL滴定管中液面的位置。如果液面处的读数是a,则滴定管中液体的体积(填代号)________。
A.是a mL B.一定大于a mL
C.是(50-a) mL D.一定大于(50-a) mL
(3)已知KMnO4、MnO2在酸性条件下均能将草酸 (H2C2O4)氧化:
(i)MnO4-+H2C2O4+H+→Mn2++CO2↑+H2O(未配平)
(ii)MnO2+H2C2O4+2H+=Mn2++2CO2↑+2H2O
某研究小组为测定某软锰矿中MnO2的质量分数,准确称取1.20g软锰矿样品,加入1.80g草酸,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液转移到容量瓶中并定容;从中取出25.00mL待测液置于锥形瓶中,再用0.020mol·L-1KMnO4标准溶液进行滴定,当滴入20.00mLKMnO4溶液时恰好完全反应。试回答下列问题:
① 方程式(i)配平后H2C2O4的计量系数为 。
② 0.020mol·L-1KMnO4标准溶液应置于 (填“甲”或“乙”)滴定管中;滴定终点的颜色变化是 。

③ 你能否帮助该研究小组求得软锰矿中MnO2的质量分数;若“能”,请给出计算结果;若“否”,试说明原因。“能”的计算结果或“否”的原因说明 。
④若在实验过程中存在下列操作,其中会使所测MnO2的质量分数偏小的是 。
A.滴定前尖嘴部分有一气泡,滴定终点时消失
B.溶液转移至容量瓶中,未将烧杯、玻棒洗涤
C.滴定前仰视读数,滴定后俯视读数
D.定容时,俯视刻度线
E.锥形瓶水洗之后未用待测液润洗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com