
(12分).已知常温下氯酸钾与浓盐酸反应放出氯气,KClO3 + 6 HCl = KCl + 3Cl2 ↑+3H2O。某校化学活动小组现按下图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的颜色棉球,反应一段时间后,观察出:
(1).对图中指定部位颜色变化为

|
|
① |
② |
③ |
④ |
|
颜色 |
|
|
|
|
(2).写出②中离子反应方程式_____________________________________.
写出④中离子反应方程式____________________________________________
(3).标出KClO3 + 6 HCl = KCl + 3Cl2 ↑+ 3 H2O反应中电子转移的方向和数目.
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
| c(B) |
| c(OH-) |
| c(OH-) |
| c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
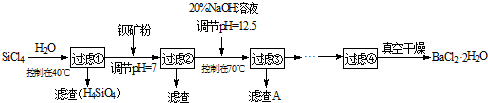
【12分】已知A为酸式盐,B为某二价主族金属元素的化合物,C、D、F、G、I在常温常压下均呈气态,且D燃烧时产生的氧炔焰常用来焊接或切割金属。等物质的量A、B与少量的水充分混合能恰好完全反应。图中反应条件(除高温外)均已略去。

(1)写出B的电子式___________,D的结构简式___________。
(2)写出A与B反应的化学方程式____________________________________。
(3)将I气体通入溶有饱和C气体的NaCl溶液,是侯氏制碱法的一步关键反应,该反应的化学方程式为___________________________________。
(4)写出下列反应的离子方程式:
①在A溶液中加入M_________________________________。
②向A溶液中加入过量NaOH溶液,并加热________________________。
③已知Fe3O4能溶于M溶液并产生F气体,该离子方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源:2009—2010学年广州市七区联考高二化学下学期期末监测 题型:计算题
(12分)
Ⅰ.已知常温下,AgCl的Ksp=1.8×10-10,AgBr的Ksp=4.9×10-13。
(1)现向AgCl的悬浊液中:
①加入AgNO3固体,则c(Cl-) (填“变大”、“变小”或“不变”,下同);
②若改加更多的AgCl固体,则c(Ag+) ;
③若改加更多的KBr固体,则c(Ag+) ,c(Cl-) ;
(2)有关难溶盐的溶度积及溶解度有以下叙述,其中正确的是 ;
| A.将难溶电解质放入纯水中,溶解达到平衡时,升高温度, Ksp 一定增大 |
| B.两种难溶盐电解质,其中Ksp小的溶解度也一定小 |
| C.难溶盐电解质的Ksp与温度有关 |
| D.向AgCl的悬浊液中加入适量的水,使AgCl再次达到溶解平衡,AgCl的Ksp不变,其溶解度也不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(08潍坊模拟)12分)已知:五种短周期元素A、B、C、D、E的原子序数依次增大。其中,元素B原子的最外层电子数是次外层电子数的2倍,元素A与D、C与E分别同主族;A、B、D、E的单质都能在C的单质中燃烧,分别生成化合物X、Y、Z、P;化合物X在常温下是一种液体,化合物Y是一种有毒气体,单质E和化合物Z都是淡黄色固体。
请回答列下问题:
(1)在周期表中,元素B位于 周期 族;E元素原子形成的简单离子的结构示意图 ;
(2)将A、B、C、D、E五种元素的原子半径按由小到大顺序排列(用元素符号表示)
(3)物质P可以使溴水褪色,写出该反应的离子方式 ;
(4)化合物X、Y、Z、P中的某两种能发生反应,生成A、B、C、D、E中的一种单质。试写出符合上述条件的两个化学方程式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com