
| A、K2C2O4溶液的电离方程式:K2C2O4?2K++C2O42- |
| B、制备乙酸乙酯时将产生的蒸气导入饱和碳酸钠溶液:CO32ˉ+2H+=CO2↑+H2O |
| C、氯化镁溶液中通入二氧化碳:Mg2++CO2+H2O═MgCO3↓+2H+ |
| D、将等体积等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、用过量的氨水除去Al3+溶液中的少量Fe3+ |
| B、用苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出 |
| C、含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热煮沸,即可得到较纯净的FeCl3溶液 |
| D、除去乙醇中少量的乙酸:加足量生石灰,蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 电极反应式 | 出现环境 | |
| A | O2+2H2O+4e-=4OH- | 碱性环境下氢氧燃料电池的负极反应 |
| B | 4OH--4e-=O2↑+2H2O | 弱酸性环境下钢铁的吸氧腐蚀的正极 |
| C | 2H++2e-=H2↑ | 用Cu作电极电解NaOH溶液的阴极反应 |
| D | H2-2e-=2H+ | 用惰性电极电解H2SO4的阴极反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1个N2分解的同时,有3个H2的形成 |
| B、1个N2分解的同时,有3个H2的分解 |
| C、1个N2分解的同时,有1个NH3的分解 |
| D、1个N2分解的同时,有2个NH3的形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
| B、乙醇、乙酸和甲醛广泛应用于食品加工 |
| C、计算机芯片所用的材料是高纯度的二氧化硅 |
| D、捕获工业排放的CO2能降低地球的温室效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溴苯中混有溴,有汽油箤取出溴 |
| B、硝基苯中混有浓HNO3和浓H2SO4,将其倒入到NaOH溶液中,静置,分液 |
| C、乙烷中混有乙烯,通氢气在一定条件下反应,使乙烯转化为乙烷 |
| D、乙烯中混有SO2和CO2,将其先后通入NaOH和KMnO4溶液洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
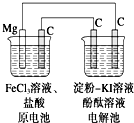 某研究性学习小组的课题为“MgC原电池电解淀粉KI溶液的研究”,其研究装置如图所示.下列有关说法不正确的是( )
某研究性学习小组的课题为“MgC原电池电解淀粉KI溶液的研究”,其研究装置如图所示.下列有关说法不正确的是( )| A、镁为负极,发生还原反应 |
| B、原电池中碳极反应式为Fe3++e-═Fe2+ |
| C、电解池中阳极处变蓝 |
| D、电解池中阴极处变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,Al与浓硫酸接触无明显现象,是由于Al与浓硫酸不反应 |
| B、SO2水溶液和氯水均具有漂白性,两者混合漂白性将增强 |
| C、已知相同温度下Ksp(BaSO4)<Ksp(BaCO3),故BaSO4无法转化为BaCO3 |
| D、CO2气体通入Na2SiO3溶液中产生白色沉淀,可说明碳元素的非金属性比硅元素强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com