
【题目】下列说法正确的是( )
A.葡萄糖和蔗糖互称同系物
B.等物质的量的甲烷和氯气反应可制取纯净的一氯甲烷
C.用NaOH溶液除去乙酸乙酯中混有的乙酸和乙醇
D.甲苯能发生氧化反应、加成反应和取代反应
科目:高中化学 来源: 题型:
【题目】分别向等体积1mol/L盐酸和1mol/L醋酸溶液中加入等量的镁条,反应时间与溶液pH变化关系如右图。下列说法中不正确的是( )

A. Y代表盐酸与镁条的反应
B. a点时反应Y消耗镁条的量少
C. b点表示此时两溶液pH相等
D. c点表示此时反应结束
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活息息相关,在各个方面都起着重要的作用。
(1)材料是经济和生态文明建设的重要物质基础。
合成塑料在生活中广泛应用,乙烯形成聚乙烯的方程式:_____________________。该反应的反应类型:_________________.橡胶是制造轮胎的重要原料,橡胶属于____________________填字母。
A金属材料 B无机非金属材料 C有机高分子材料
铝热反应在工业生产中的重要用途之一是焊接钢轨,其反应的化学方程式为:______________________________________;钢铁制品在潮湿的空气中能发生腐蚀,发生该腐蚀时的负极反应式为__________________________________。
(2)“三高症”是指高血糖糖尿病、高血脂和高血压症,是现代社会中的“富贵病”。
①血糖是指血液中的葡萄糖。葡萄糖的结构简式是__________________________。在加热条件下,加入氢氧化钠溶液,调节溶液为碱性,此时葡萄糖与新制的氢氧化铜发生反应,观察到的现象是________________此方法曾经用于检测糖尿病。
②血脂是血液中所含脂类物质的总称。油脂对人体的作用之一是________,但过量摄入,可能引起肥胖、高血脂、高血压。油脂在碱性条件下水解反应称为_____________.
③高血压可由肥胖、糖尿病、摄入过多钠盐等引起,而摄入过量的蛋白质也会造成脂肪堆积。蛋白质水解的最终产物是________,蛋白质的组成元素除C、H、O外,还含有_______(填一种)。
(3)石油在生活中的应用广泛。石油是由多种碳氢化合物组成的混合物,从原油中分离出汽油、煤油、柴油等轻质油的方法是____________________(填操作名称).分离出的汽油_______(填“是”或者“否”)可作萃取剂。汽油是C5~C11的混合烃,其中含有5个碳原子的烷烃存在________种同分异构体,其中一种同分异构体的一氯代物只有一种,则该同分异构体与氯气发生取代反应生成一氯代物的化学方程式为:___________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期主族元素 W、M、X、Y、Z 原子序数依次增大,请结合表中信息回答下列问题:
元素 | W | M | X | Y | Z |
结构或性质 | 最高价含氧 酸与其气态 氢化物能发 生化合反应 | 氢化物的水 溶液能刻蚀 玻璃 | 焰色反应火 焰呈黄色 | 同周期主族元 素形成的简单 离子中,其离子 半径最小 | 最高正价与 最低负价代 数和为 6 |
(1)M元素在周期表中的位置为_____。
(2)M、X、Z元素所对应简单离子半径由大到小的顺序为_____________________(用离子符号表示)。
(3)W最高价含氧酸与其气态氢化物发生化合反应生成的物质中含有的化学键类型为___________________________________。
(4)下列可作为比较M和Z的非金属性强弱的依据是_________(填序号)。
A.单质与H2反应的难易程度
B.氢化物的稳定性
C.最高价氧化物的水化物酸性强弱
D.将M的单质通入Z的钠盐溶液观察是否有Z逸出
(5)W能形成多种氢化物,其中一种氢化物可作为火箭燃料,该物质中W与氢元素的质量比为7:1,写出该氢化物的电子式______。该氢化物和 O2 在碱性条件下可形成燃料电池,产生两种无毒物质,写出其负极的电极反应式___________.
(6)Y元素和W元素形成的化合物YW一种新型无机材料,可与过量烧碱溶液反应产生使湿润的红色石蕊试纸变蓝的气体,写出有关的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,改变反应物中n(SO2)对反应2SO2(g)+O2(g) 2SO3(g) △H<0的影响如图所示,下列说法正确的是
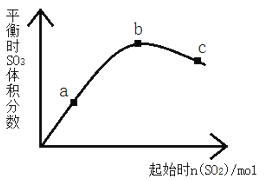
A. 反应b、c点均为平衡点,a点未达平衡且向正反应方向进行
B. a、b、c三点中,a点时SO2的转化率最高
C. 反应a、b、c点均为平衡点,b点时SO2的转化率最高
D. a、b、c三点的平衡常数Kb>Kc>Ka
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 向明矾溶液中加入过量氢氧化钡溶液:SO42-+Ba2+ ![]() BaSO4↓
BaSO4↓
B. 向CH3COOH中加入足量的氢氧化钠溶液: CH3COOH+OH- ![]() CH3COO-+H2O
CH3COO-+H2O
C. 向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2 +2H+![]() Fe2++2H2O
Fe2++2H2O
D. 向碳酸氢铵溶液中加入足量的氢氧化钠溶液:NH4++ OH- ![]() NH3·H2O
NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“一碳化学”是指以含一个碳原子的化合物(如:CO2、CO、CH4、CH3OH等)为初始反应物,合成一系列重要的化工原料和燃料的化学。以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应I:2NH3(g)+CO2(g)![]() NH2COONH4(s) △H1=-159.47kJ/mol K1
NH2COONH4(s) △H1=-159.47kJ/mol K1
反应II:NH2COONH4(s)![]() CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol K2
CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol K2
总反应:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g) △H3 K3
CO(NH2)2(s)+H2O(g) △H3 K3
请回答:
(1)①总反应的△H3=_______kJ/mol。该热化学方程式的平衡常数K3=______(用K1、K2表示)。
②一定温度下,在体积固定的密闭容器中按计量比进行反应I,下列不能说明反应达平衡状态的是_____________。
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.2V正(NH3)=V逆(CO2)
D.容器内混合气体的密度不再变化
③环境为真空时,在一敞开容器(非密闭容器)中加入NH2COONH4固体,足够长时间后,反应是否建立平衡状态? ___________(填“是”或“否”)。
(2)在体积可变的恒压 (P总) 密闭容器中充入1 mol CO2 与足量的碳,让其发生反应:C(s)+ CO2(g)![]() 2CO(g) △H>0。平衡时,体系中气体体积分数与温度的关系如下图所示。
2CO(g) △H>0。平衡时,体系中气体体积分数与温度的关系如下图所示。
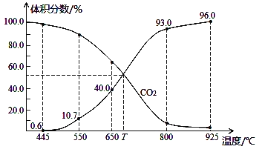
①T℃时,达平衡后向容器中若充入稀有气体,v(正)___v(逆) (填“>”“<”或“=”);若充入等体积的CO2 和CO,平衡________移动(填“正向”“逆向”或“不”)。
②650℃,CO2 的转化率为_____________。
③已知:气体分压(P分)=气体总压×体积分数。用平衡分压代替平衡浓度表示平衡常数,925℃时,Kp=_____________ (用含P总的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作不正确的是
A. 蒸发时,残留的少量水让余热蒸干
B. 分液时,下层液体从下端放出,上层液体从上端倒出
C. 蒸馏时,冷水从冷凝管上口进下口出
D. 过滤时,漏斗下端紧贴烧杯内壁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com