
| m |
| M |
| 15.8g |
| 158g/mol |
| 0.5mol |
| 1 |
| 0.5mol |
| 2 |


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
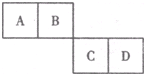 已知A、B、C、D四种短周期元素在元素周期表中的相对位置如图所示,它们的原子序数之和为46.请填空:
已知A、B、C、D四种短周期元素在元素周期表中的相对位置如图所示,它们的原子序数之和为46.请填空:查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)实验室电解饱和食盐水时发生反应的化学方程式为
(1)实验室电解饱和食盐水时发生反应的化学方程式为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
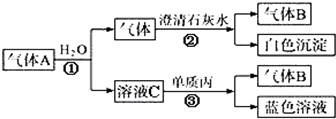
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠通常保存在石蜡油或煤油中 |
| B、新制氯水通常保存在棕色试剂瓶中 |
| C、氢氧化钠溶液通常保存在带有橡皮塞的玻璃瓶中 |
| D、氢氟酸通常保存在玻璃瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com